
| A. | 随着电子层数增多,碱金属的原子半径逐渐增大 | |
| B. | 碱金属具有强还原性,它们的离子具有强氧化性 | |
| C. | 碱金属单质的熔沸点随着核电荷数的增大而降低 | |
| D. | 碱金属元素在自然界中都是以化合态存在的 |
分析 A.随着原子序数增多,碱金属原子的电子层数越多;
B.碱金属阳离子达到稳定结构,性质稳定;
C.根据影响金属晶体熔沸点高低的因素判断;
D.碱金属性质活泼,容易与空气中水、氧气反应.
解答 解:A.随着原子序数增多,碱金属原子的电子层数越多,则原子半径随原子序数增大而逐渐增大,故A正确;
B.碱金属阳离子达到稳定结构,性质稳定,不具有强的氧化性,故B错误;
C.原子半径Li<Na<K<Rb<Cs,晶体结构相似,则原子半径越大,金属键越弱,单质的熔沸点越低,故C正确;
D.碱金属性质活泼,容易与空气中水、氧气反应,所以碱金属元素在自然界中都是以化合态存在的,故D正确;
故选:B.
点评 本题考查了碱金属的性质,熟悉同主族元素性质的递变规律是解题关键,注意金属晶体熔沸点影响因素,题目难度中等.


科目:高中化学 来源: 题型:实验题
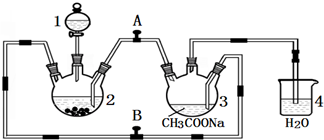
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U互为同位素 | |
| B. | ${\;}_{94}^{238}$Pu与${\;}_{94}^{239}$Pu最外层电子数相同 | |
| C. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U化学性质完全相同 | |
| D. | ${\;}_{94}^{238}$Pu与${\;}_{94}^{239}$Pu互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
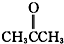 酮类 ③CH3CH2Br卤代烃
酮类 ③CH3CH2Br卤代烃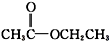 酯类 ⑤
酯类 ⑤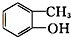 酚类 ⑥
酚类 ⑥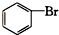 卤代烃
卤代烃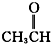 醛类 ⑧
醛类 ⑧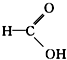 羧酸类 ⑨
羧酸类 ⑨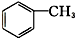 芳香烃.
芳香烃.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
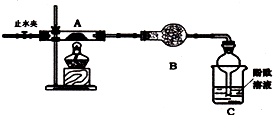

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
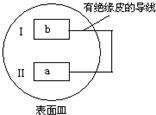 把活泼金属片a和b放在盛有稀食盐水和酚酞混合液的表面皿中,构成如图所示原电池,一段时间后观察到区域I变红色,则下列叙述正确的是( )
把活泼金属片a和b放在盛有稀食盐水和酚酞混合液的表面皿中,构成如图所示原电池,一段时间后观察到区域I变红色,则下列叙述正确的是( )| A. | a是原电池的负极 | B. | b的活泼性大于a | ||
| C. | 无电流产生 | D. | b 电极上有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
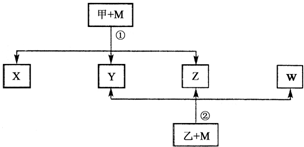
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池放电时正极反应为VO2++2H++e-═VO2++H2O | |
| B. | 充电时阴极反应为V2+-e-═V3+ | |
| C. | 电解池的阴极反应式为3O2+6H2O+6e-═3H2O2+6OH- | |
| D. | 电解池中生成22.4 L O3(标准状况)时,转移3 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com