
| 醋酸浓度(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
 ____________________________________
____________________________________科目:高中化学 来源:不详 题型:单选题
| A.醋酸能与大理石反应产生二氧化碳气体 |
| B.pH = 3的醋酸溶液稀释100倍后pH<5 |
| C.室温下,醋酸钠溶液的pH>7 |
| D.常温下,0.1 mol·L-1醋酸溶液pH="2.5" |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
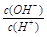 =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 _____,B1__________,B2__________;
_____,B1__________,B2__________; 度相等时,两溶液中水电离出的氢离子的物质的量浓度之比为_______________________ _;
度相等时,两溶液中水电离出的氢离子的物质的量浓度之比为_______________________ _;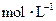 的
的 溶液中离子浓度大小排序 ________________;
溶液中离子浓度大小排序 ________________;查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
A.挥 发性 发性 | B.酸性比碳酸强 | C.难电 离 离 | D.易溶于水 |

 的比值 (填“增大”、“减小”或“不变”)。
的比值 (填“增大”、“减小”或“不变”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加热 | B.加入1mol/L 的醋酸溶液100mL |
| C.加入少量的0.5mol/L的硫酸 | D.加入少量的1mol/L 的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
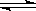 CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是( )
CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是( )| A.NH4Cl固体 | B.CH3COONa | C.NH3·H2O | D.Zn粉 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通过测浓度均为0.01 mol/L的溶液的pH大小来鉴别盐酸和乙酸? |
| B.向均含石蕊的盐酸和乙酸溶液中分别加入NaCl、CH3COONa来鉴别盐酸和乙酸是否为弱电解质? |
| C.加热蒸发FeCl3溶液制备FeCl3晶体? |
| D.测均为0.1 mol/L的NaCl、CH3COONa溶液的pH来鉴别盐酸和乙酸是否为弱电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com