
(1)能源就是能提供__________的__________,它包括化石燃料、__________、__________、__________、__________以及柴草等。化石燃料包括__________、__________和__________。
(2)我国目前的能源利用状况
①我国目前使用的重要能源是__________,它们的蕴藏量__________,而且不能__________,最终将会__________。
②基于我国目前的__________水平和__________水平,能源从开采、运输、加工到终端的利用效率都__________,浪费__________。据统计,总效率仅为__________。
(3)解决方法
①提高现有能源的利用率
加强__________投入,提高__________水平,改善开采、运输、加工等各个环节,科学地控制燃烧反应,使燃料__________燃烧,提高能源的__________。
②开发新的能源
现在探索的新能源主要有__________、__________、__________、地热能、海洋能和生物质能等。它们的特点是资源__________,__________再生,__________污染或__________污染。
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
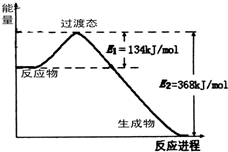 能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料.
能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料. 查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | 键能(kJ/mol) | 化学键 | 键能(kJ/mol) |
| N≡N | 942 | H-O | 460 |
| N-H | 391 | O=O | 499 |
| H-H | 437 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为缓解能源危机,能源专家构想出了利用太阳能促使燃料循环的构想图:

当前,科学家还未实现这一构想。但大自然已经解决了这个问题,绿色植物的光合作用就是在日光作用下,利用太阳能把CO2和H2O转变成了能源葡萄糖(可燃烧): 6CO2 + 6H2O![]() C6H12O6 + 6O2
C6H12O6 + 6O2
(1)如果上述构想成立,试写出有关反应的化学方程式。
(2)在此构想的物质循环中,太阳能最终转化为___________能。
(3)实现上述构想的关键问题是什么?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com