
A.CH3 B.CH C.CH2 D.CH4?
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:阅读理解


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
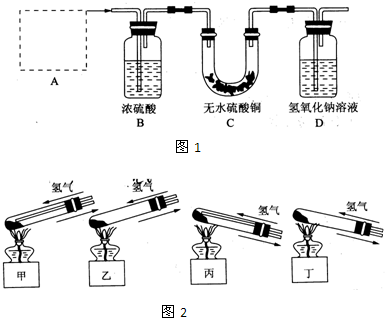
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
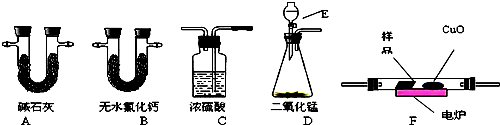
查看答案和解析>>
科目:高中化学 来源:2011-2012学年辽宁省盘锦市二中高二下学期期中考试化学试卷(带解析) 题型:实验题
( 1 ) (4分)在实验室鉴定氯酸钾晶体和1-氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加入NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取残渣;⑦用HNO3酸化。
鉴定氯酸钾中氯元素的操作步骤依次是_______________ (填序号)
鉴定1-氯丙烷中氯元素的操作步骤依次是_____________ (填序号)
( 2 ) (11分)通常用燃烧的方法测定有机物的的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的的质量确定有机物的组成。下图所示的是用燃烧法确定有机物分子式的常用装置。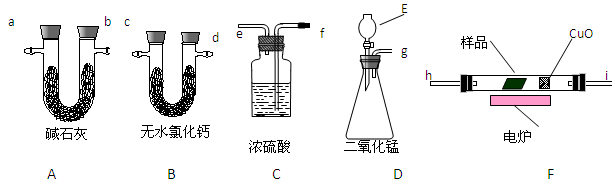
现准确称取1.8g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重1.76g,
B 管增重0.36g。请回答:
(1)该有机物的的最简式为__________________;
(2)产生的气体由左向右流向,所选用的各导管口连接的顺序是____________;
(3)E中应盛装什么试剂:_______________;
(4)如果把CuO网去掉,A管重量将_____________;(填“增大”、“减小”、或“不变”)
(5)A、B管内均盛有有固态试剂,B管的作用是______________________;
(6)要确定该有机物的分子式,还必须知道的数据是___________;
A. 消耗液体E的质量 B. 样品的摩尔质量 C. CuO固体减少的质量
D. C装置增加的质量 E. 燃烧消耗O2的物质的量
(7)在整个实验开始之前,需先让D产生的气体通过整套装置一段时间,其目的是
__________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com