
(14分)某学习小组的同学在学习了Na2CO3、NaHCO3的性质后,了解到它们都能与盐酸反应产生CO2气体,那么如何鉴别Na2CO3和NaHCO3呢?带着这样的疑问,他们进行了下列探究:
【猜想】(1)甲同学认为可用CaCl2溶液鉴别Na2CO3和NaHCO3溶液,而不能用澄清石灰水鉴别。
(2)乙同学认为固体Na2CO3、NaHCO3可用加热的方法鉴别。
依据是 。
(3)丙同学认为可用盐酸鉴别Na2CO3和NaHCO3固体。
【实验探究】
(1)甲同学:①将CaCl2溶液加入到分别盛有少量Na2CO3、NaHCO3溶液的试管中,发现盛有Na2CO3的试管产生了白色沉淀;②将澄清石灰水加入到分别盛有少量Na2CO3、NaHCO3溶液的试管中,发现两支试管中也都产生了白色沉淀。
此实验结果与猜想相同。
(2)乙同学分别取了一定量的Na2CO3、NaHCO3固体于大试管中加热(如图1):
①加热Na2CO3时,开始即见小试管中有少量气泡产生,继续加热,气泡逐渐减少,未见澄清石灰水变浑浊,
②加热NaHCO3时,乙同学观察到实验现象与①不同,证实了自己的猜想是合理的。
(3)丙同学在两支分别盛有少量Na2CO3、NaHCO3固体的试管中,各加入2 mL
2 mol/L的盐酸,观察到两支试管中均产生了大量气体,实验结果与猜想不一致,即得出不能用盐酸鉴别Na2CO3和NaHCO3。
【问题讨论】
(1)甲同学的两个实验中,大家对CaCl2与Na2CO3溶液的反应比较熟悉,该反应的离子方程式为 ;
(2)乙同学在加热Na2CO3固体时,开始产生少量气泡的原因是 ;在加热NaHCO3固体时,乙同学观察到的实验现象是 。
(3)丁同学认为丙同学的结论不对。丁同学认为对实验方案做一些改进,可用于鉴别碳酸钠与碳酸氢钠。他的改进方法是:称取各2.1 g两种固体,放入两个容积一样的气球中,在两只锥形瓶中各加入约25 mL 2 mol/L 的盐酸,分别将气球套在锥形瓶瓶口上,同时将气球中的固体同时倒入锥形瓶中,气球的膨胀比较 (填快或慢)的或最后气球比较 (填大或小)的是碳酸氢钠。
【拓展应用】
(1)要除去Na2CO3溶液中混有的少量NaHCO3,可加入适量的 溶液。
(2)要测定Na2CO3与NaHCO3固体混合物中Na2CO3的质量分数,可采用的方案有多种,请简述其中一种方案(写出简要步骤及要测定的数据,不要求写出如何用数据求出结果):
。
【猜想】
(2)NaHCO3不稳定,受热易分解,而Na2CO3受热不易分解。(或用方程式表示也可)
【问题讨论】
(1)CO32-+Ca2+=CaCO3↓
(2)空气受热膨胀
澄清石灰水变浑浊、小试管中有大量气泡产生、大试管管口有水珠等(写出两个现象即可)
(3)快 大
【拓展应用】(1)NaOH(或氢氧化钠)
(2)方案一:称取5 g样品于坩埚(已称量)加热至无水蒸气逸出,冷却、称量加热后样品与坩埚的质量,重复至恒重。
方案二:称取5 g样品于已称质量的烧杯中,加入已称质量的50mL 2mol/L的硫酸,充分搅拌后,静置,称量烧杯(含反应后溶液)的质量至恒重。
方案三:称取5 g样品于已称质量的烧杯中,加入50mL 2mol/L的氢氧化钡溶液,充分搅拌后,静置,过滤、洗涤、烘干沉淀,冷却称量沉淀的质量。
方案四:称取5 g样品于烧杯中,加入50mL 蒸馏水,充分搅拌后,称量烧杯(含溶液)的质量,然后通入纯净干燥的二氧化碳,充分反应后,再称量至恒重。
(写出一种其它合理方案都给分,使用CaCl2或BaCl2不得分)
解析


科目:高中化学 来源: 题型:阅读理解
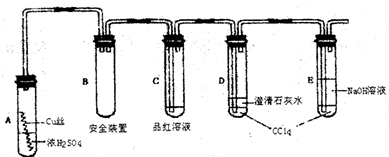
| ||
| ||
| ||
 Cu(OH)2+2H+
Cu(OH)2+2H+ Cu(OH)2+2H+
Cu(OH)2+2H+查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
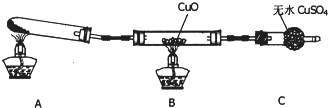
| H+ |
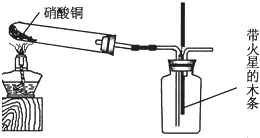
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)(一)铝是生活中非常常见的一种金属,运用所学知识回答:
(1)金属铝是活泼的金属,但在生活中应用很广泛,原因是 。
(2)铝盐或铁盐能用于净水,是因为铝盐或铁盐在水溶液中形成了 。
(3)铝粉与氧化铁粉末在高温下得到铁的反应叫做“铝热反应”,发生反应的化学方程式为 。
(二)有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸。某研究性学习小组的同学们利用一小块样品,设计实验证明矿物样品中有Fe3+。
实验用品:研钵、烧杯、玻璃棒、漏斗、铁架台、滤纸、试管、胶头滴管
(4)简述实验操作步骤、现象和结论。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年广东省实验中学高一上学期期末考试化学试卷 题型:填空题
(10分)(一)铝是生活中非常常见的一种金属,运用所学知识回答:
(1)金属铝是活泼的金属,但在生活中应用很广泛,原因是 。
(2)铝盐或铁盐能用于净水,是因为铝盐或铁盐在水溶液中形成了 。
(3)铝粉与氧化铁粉末在高温下得到铁的反应叫做“铝热反应”,发生反应的化学方程式为 。
(二)有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸。某研究性学习小组的同学们利用一小块样品,设计实验证明矿物样品中有Fe3+。
实验用品:研钵、烧杯、玻璃棒、漏斗、铁架台、滤纸、试管、胶头滴管
(4)简述实验操作步骤、现象和结论。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com