
| A.稀硝酸 | B.盐酸 | C.浓硫酸 | D.稀硫酸 |


科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
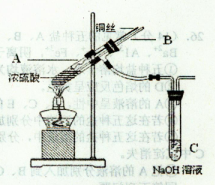
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定条件下,铁粉可与水蒸气反应 | B.不锈钢是铁的合金,只含金属元素 |
| C.铁与盐酸反应,铁的合金不与盐酸反应 | D.在空气中,铁板比镀锌铁板更耐腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.I和III | B.I和IV |
| C.II和III | D.II和IV |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入KSCN的溶液一定不变红色 | B.溶液中一定含Cu2+ |
| C.溶液中一定含有Fe2+ | D.剩余固体中一定有铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由上述反应可知,Fe(OH)3的氧化性强于FeO42— |
| B.高铁酸钾中铁显+6价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为3: 2 |
| D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com