
【化学——选修2:化学与技术】(15分)工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收。请回答下列问题:
(1)煅烧黄铁矿形成的炉气必须经除尘、洗涤、干燥后进入 (填设备名称),其主要目的是 。
(2)催化氧化所使用的催化剂钒触媒(V2O5)能加快二氧化硫氧化速率,此过程中产生了一连串的中间体(如图),其中a、c二步反应的化学方程式可表示为: 、 。
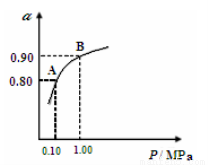
(3)550℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(P)的关系如图所示,则:将2.0mol SO2和1.0mol O2置于5L密闭容器中,反应达平衡后,体系总压强为0.10M Pa,A与B表示不同压强下的SO2转化率,通常情况下工业生产中采用常压的原因是: 。
(4)为循环利用催化剂,科研人员最新研制了一种离子交换法回收钒的新工艺,回收率达91.7%以上。已知废钒催化剂中含有V2O5、VOSO4及不溶性残渣,查阅资料知:VOSO4可溶于水,V2O5难溶于水,NH4VO3难溶于水。该工艺的流程如图如下:
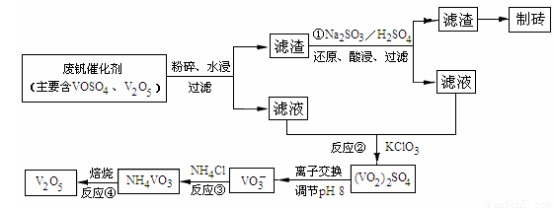
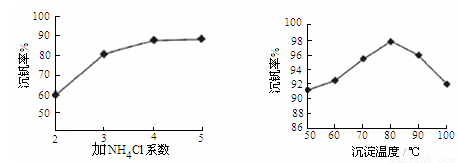
则反应①②③④中属于氧化还原反应的是 (填数字序号),反应①的离子方程式为 ,该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据下图试建议控制氯化铵系数和度: 、 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,11.2 L CCl4中含有的分子数为0.5 NA
B.1 mol Cl2完全溶于水,转移的电子数为NA
C.25°C时,pH=13的1.0 L Ba(OH)2溶液中含有的OH数为0.1 NA
D.电解精炼铜,转移2 NA个电子时,阳极溶解64 g铜
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长沙市高三4月月考理综化学试卷(解析版) 题型:选择题
化学与人类社会的生产、生活有着密切联系。下列叙述中正确的是
A.苹果放在空气中久置变黄和纸张久置变黄原理相似
B.用活性炭为蔗糖脱色和用臭氧漂白纸浆,原理相似
C.钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀
D.黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高三3月教学质量监测理综化学试卷(解析版) 题型:简答题
(15分)焦炭与CO、H2均是重要的能源,也是重要的化工原料。
(1)已知C、H2、CO的燃烧热(△H)分别为-393.5 kJ·mol-1、-285.8kJ·mol-1、-283 kJ·mol-1,又知水的气化热为+44 kJ/mol。
①焦炭与水蒸气反应生成CO、H2的热化学方程式为___________________。
②若将足量焦炭与2mol水蒸气充分反应,当吸收能量为191.7 kJ时,则此时H2O(g)的转化率为_________________。
(2)将焦炭与水蒸气置于容积为2L的密闭容器中发生反应:C(s)+H2O(g) CO(g)+H2(g),其中H2O、CO的物质的量随时间的变化曲线如图所示。
CO(g)+H2(g),其中H2O、CO的物质的量随时间的变化曲线如图所示。
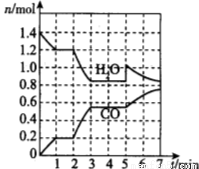
①第一个平衡时段的平衡常数是______________,若反应进行到2 min时,改变了温度,使曲线发生如图所示的变化,则温度变化为___________(填“升温”或“降温”)。
②反应至5 min时,若也只改变了某一个条件,使曲线发生如图所示的变化,该条件可能是下述中的____。
a.增加了C
b.增加了水蒸气
c.降低了温度
d.增加了压强
(3)假设(2)中反应在第2min时,将容器容积压缩至1 L,请在上图中绘制出能反映H2O、CO物质的量变化趋势的图像。
(4)若以CO、O2、K2CO3等构成的熔融盐电池为动力,电解400 mL饱和食盐水,则负极上的电极反应式为______________________,当有5·6g燃料被消耗时,电解池中溶液的pH=__________(忽略溶液的体积变化,不考虑能量的其它损耗)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高三3月教学质量监测理综化学试卷(解析版) 题型:选择题
某有机物的结构简式如图所示,下列有关该有机物的说法中正确的是
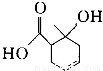
A.能和碳酸钠溶液反应的官能团有2种
B.1mol该有机物最多能与2molH2发生加成
C.与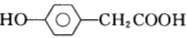 互为同分异构体
互为同分异构体
D.既可以发生取代反应又可以发生氧化反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省新校高三4月模拟化学试卷(解析版) 题型:选择题
电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。下列叙述中正确的是

A.A膜是阳离子交换膜
B.通电后,海水中阴离子往b电极处运动
C.通电后,a电极的电极反应式为4OH--4e-===O2↑+2H2O
D.通电后,b电极上产生无色气体,溶液中出现白色沉淀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省淮北市高三第二次模拟考试理综化学试卷(解析版) 题型:实验题
(14分)锗及其化合物被广泛应用于半导体、催化剂等领域。以铅锌矿含锗烟尘为原料可制备GeO2,其工艺流程图如下。
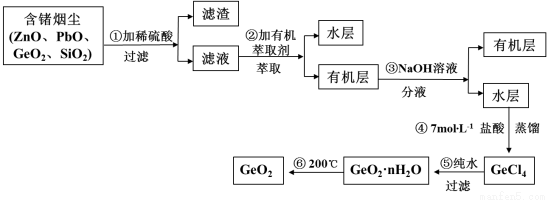
已知:GeO2是两性氧化物;GeCl4易水解,沸点86.6℃
(1)第①步滤渣主要成分有 (填化学式),实验室萃取操作用到的玻璃仪器有 。
(2)第③步萃取时,锗的萃取率与V水相/V有机相(水相和有机相的体积比)的关系如下图所示,
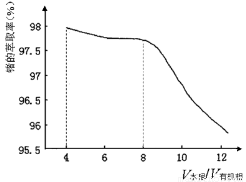
从生产成本角度考虑,较适宜的V水相/V有机相的值为 。
(3)第④步加入盐酸作用 (答两点即可)。
(4)第⑤步反应的化学方程式 。
(5)检验GeO2·nH2O是否洗涤干净的操作是 。
(6)GeO2产品中通常混有少量SiO2。取样品5.4g,测得其中氧原子的物质的量为0.105mol,则该样品中GeO2的物质的量为_____ mol。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省黄山市高三毕业班第二次质量检测理综化学试卷(解析版) 题型:选择题
电解Na2SO4溶液生Na2SO4和烧碱的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1:2,下列有关说法正确的是(说明:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)
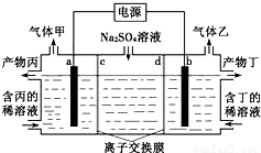
A.a极反应式为:2H++2e一=H2↑
B.产物丁为NaOH
C.c为阳离子交换膜
D.每转移0. 2mol电子,产生l 12L气体甲
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:填空题
(8分)X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+3、+5、+7,核电荷数按照Z、X、Y、W的顺序增大。已知Z的原子次外层的电子数为2,W、X原子次外层电子数为8。
(1)元素W在周期表中的位置 。
(2)用电子式表示X在空气中生成的氧化物的形成过程: 。
(3)X、Y、Z、W的原子半径由大到小的顺序为: 。(用元素符号表示)
(4)请写出W的单质与X的最高价氧化物对应水化物反应的离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com