
已知H2O2在催化剂作用下分解速率加快,进程的变化示意图。下列说法正确的是
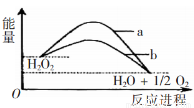
A.加入催化剂,可提高H2O2的平衡转化率
B.a表示的催化剂效率高于b表示的催化剂效率
C.改变催化剂.既能改变反应热.也能改变活化能
D.该反应可自发进行
科目:高中化学 来源:2017届四川省成都市高三上学期一诊化学试卷(解析版) 题型:选择题
常温下,将0.1L0.1mol/L Na2S2O3溶液与一定量的pH=2的硫酸溶液混合,放出VL气体。NA代表阿伏加德罗常数的值,下列说法正确的足
A.pH=2的硫酸溶液含有H+数目为0.0lNA
B.该反应释放SO2分子数目为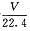 NA
NA
C.反应中每摩尔Na2S2O3转移的电子数目为4NA
D.若98gH2SO4溶于水完全电离,其断裂的共价键数目为2NA
查看答案和解析>>
科目:高中化学 来源:2017届湖南省郴州市高三上第二次教学质量监测化学卷(解析版) 题型:实验题
兰尼镍是一种带有多孔结构的细小品粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的T艺流程如下图所示:
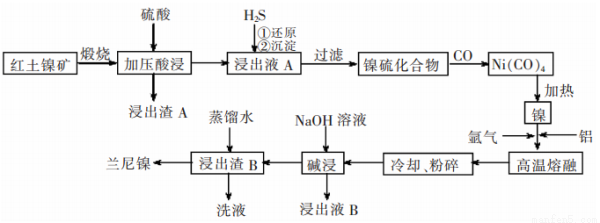
(1)在形成Ni(CO)4的过程中,碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为________;
(2)已知红土镍矿煅烧后生成固体产物为Ni2O3和Fe2O3,而加压酸浸后浸出液A中含有Ni2+,写出有关镍元素的加压酸浸的化学反应方程式____________;
(3)“碱浸”的目的是使镍产生多孔结构,从而增强对氢气的强吸附性,此过程中发生反应的离子方程式为__________。
(4)浸出液B可以回收,重新生成铝以便循环利用。请设计简单的回收流程:浸出液B→_______________。
(示例: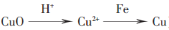 )
)
查看答案和解析>>
科目:高中化学 来源:2017届湖南省郴州市高三上第二次教学质量监测化学卷(解析版) 题型:选择题
常温下,向20mL 0.2mol/LH2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示。根据图示判断,下列说法正确的是
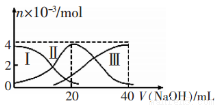
A.当V(NaOH)=20 mL时,溶液中离子浓度大小关系: c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-)
B.等浓度的NaOH溶液与H2A溶液按体积2:1混合后,其溶液中水的电离程度比纯水大
C.NaHA溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A)
D.向上述加入20 mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少
查看答案和解析>>
科目:高中化学 来源:2017届湖南省郴州市高三上第二次教学质量监测化学卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在0.01mol/LBa(OH)2溶液中:Al3+、NH4+、NO3-、HCO3-
B.0.1 mol/L的FeCl2溶液中:H+、Al3+、SO42-、ClO-
C.滴加KSCN溶液显红色的溶液:NH4+、K+、Cl-、I-
D.由水电离产生的c(H+)=l×l0-3mol/L的溶液中:Na+、B a2+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省铁岭市协作体高三上联考四化学试卷(解析版) 题型:选择题
在体积恒定的密闭容器中,一定量的SO2与1.25mol O2在催化剂作用下加热到600℃发生反应:2SO2(g)+O2(g) 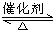 2SO3(g) △H<0。当气体的物质的量减少0.45mol时反应达到平衡,在相同的温度下测得气体压强为反应前的80%。下列有关叙述正确的是( )
2SO3(g) △H<0。当气体的物质的量减少0.45mol时反应达到平衡,在相同的温度下测得气体压强为反应前的80%。下列有关叙述正确的是( )
A.该温度下的平衡常数为101.25 L/moL
B.达到平衡时,SO2的转化率是90%
C.降低温度,正反应速率减小程度比逆反应速率减小程度大
D.将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量一定为231.4g
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省铁岭市协作体高三上联考四化学试卷(解析版) 题型:选择题
我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指( )
A.氨水 B.硝酸 C.醋 D.卤水
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一12月月考化学试卷(解析版) 题型:选择题
极据下列反应判断微粒的还原性由强到弱的顺序正确的是( )
①Cl2+2KI=I2+2KCl ②2FeCl3+2KI=I2+2FeCl2+2HCl
③2FeCl2+ Cl2=2FeCl3 ④I2+SO2+2H2O=2HI+H2SO4
A.Cl->I->Fe2+>SO2 B.Fe2+>Cl->I->SO2
C.SO2>I->Fe2+>Cl- D.SO2>Fe2+ I->Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com