
下列表格中的各种情况,可以用如图所示曲线表示的是
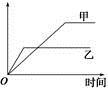
选项 | 反应 | 纵坐标 | 甲 | 乙 |
A | 相同质量的氨气,在同一容器中发生反应:2NH3 | 氨气的转化率 | 500 ℃ | 400 ℃ |
B | 等质量的钾、钠分别与足量的水反应 | H2的质量 | 钠 | 钾 |
C | 在体积可变的恒压容器中,体积之比为1∶3的N2、H2:N2+3H2 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2 mol SO2和1 mol O2在相同温度下发生反应:2SO2+O2 | SO3的物质的量 | 2个大气压 | 10个大气压 |
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源:2014高考名师推荐化学原电池四种型与金属腐蚀、保护(解析版) 题型:填空题
能量之间可相互转化:
(1)电解食盐水制备Cl2是将电能转化为化学能,而原电池可将化学能转化为电能。设计两种类型的原电池,探究其能量转化效率。限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。
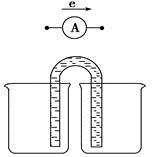
①完成原电池甲的装置示意图(见上图),并作相应标注,要求:在同一烧杯中,电极与溶液含相同的金属元素。
②以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极__________。
③甲乙两种原电池可更有效地将化学能转化为电能的是________,其原因是______________________________。
(2)根据牺牲阳极的阴极保护法原理,为减缓电解质溶液中铁片的腐蚀,在(1)的材料中应选__________作阳极。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学平衡常数(解析版) 题型:选择题
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)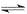 Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是
Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是
温度℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
A.上述生成Ni(CO)4(g)的反应为吸热反应
B.25℃时反应Ni(CO)4(g)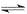 Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
C.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)>v(逆)
D.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2mol/L
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学平衡图像(解析版) 题型:选择题
对于可逆反应N2(g)+3H2(g)  2NH3(g) ΔH<0。下列研究目的和图示相符的是
2NH3(g) ΔH<0。下列研究目的和图示相符的是
| A | B | C | D |
研究 目的 | 温度(T)对反应的影响(T2>T1) | 压强(p)对平衡常数的影响 | 温度(T)对反应的影响 | 压强(p)对反应的影响(p2>p1) |
图示 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学平衡图像(解析版) 题型:选择题
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3-(aq);某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法中不正确的是
I3-(aq);某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法中不正确的是

A.反应I2(aq)+I-(aq) I3-(aq)的△H<0
I3-(aq)的△H<0
B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1﹥K2
C.若反应进行到状态D时,一定有v正﹤v逆
D.状态A与状态B相比,状态B的c(I2)大
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学实验的基本操作(解析版) 题型:选择题
无论在化学实验室还是在家中进行实验或探究活动,都必须注意安全。下列实验操作正确的是
A.用蒸发皿加热NaCl溶液
B.不慎将汞滴落到桌面上,应立即用较多的水冲洗
C.从试剂瓶中取出的一些Na2CO3溶液放入试管中,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
D.用瓷坩埚熔化氢氧化钠
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学实验的基本操作(解析版) 题型:选择题
下列实验操作正确且能达到预期目的的是
| 实验目的 | 操作 |
A | 检验淀粉水解产物有还原性 | 淀粉溶液和稀H2SO4混合加热,冷却后,再加新制的Cu(OH)2悬浊液加热至沸腾 |
B | 证明SO2具有漂白性 | 将SO2通入溴水中 |
C | 为了提取溴水中的溴 | 加入植物油进行萃取 |
D | 浓、稀HNO3分别与Cu反应 | 比较浓、稀HNO3的氧化性强弱 |
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学制备实验方案的设计与评价(解析版) 题型:实验题
可用如图所示装置制取、净化、收集的气体是
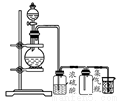
A.锌和稀硝酸反应制一氧化氮
B.亚硫酸钠与浓硫酸反应制二氧化硫
C.铁和稀硫酸反应制氢气
D.浓氨水和生石灰反应制取氨气
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学乙醇和乙酸(解析版) 题型:选择题
某品牌白酒中含有的塑化剂的主要成分为邻苯二甲酸二丁酯,其结构简式为
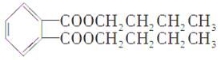
下列有关说法正确的是
A.邻苯二甲酸二丁酯的分子式为C16H21O4
B.邻苯二甲酸二丁酯属于酯类,可增加白酒的香味,对人体无害
C.用邻苯二甲酸与丁醇合成邻苯二甲酸二丁酯的反应属于取代反应
D.邻苯二甲酸二丁酯不能发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com