
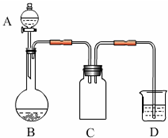
 (2012?南京模拟)实验室一般用回收的粗铜屑(含少量Cu2O)与H2SO4、HNO3混合稀溶液反应制备CuSO4?5H2O晶体,反应可在如图所示装置中进行.
(2012?南京模拟)实验室一般用回收的粗铜屑(含少量Cu2O)与H2SO4、HNO3混合稀溶液反应制备CuSO4?5H2O晶体,反应可在如图所示装置中进行.| 0.04×64 |
| 3.28 |


科目:高中化学 来源: 题型:
| 氧气 |
| 点燃 |
| 硫酸 |
| 氢氧化钠 |
| 盐酸 |
| 电解 |
| 氢氧化钠 |
| 氧气 |
| 点燃 |
| 水 |
| 水 |
| 氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:








 )是一种重要的医药中间体.写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选).
)是一种重要的医药中间体.写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选).查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com