
| A、NaNO3和浓硫酸制HNO3:Na2SO4 | B、CaF2和硫酸制HF:CaSO4 | C、NaBr、乙醇和浓硫酸制C2H5Br:NaHSO4 | D、FeS和稀硫酸制H2S:FeSO4 |


 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:阅读理解
| 无水AlCl3 |
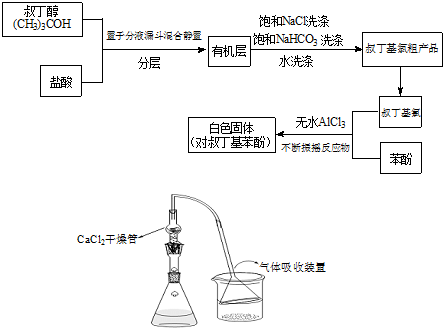
 +(CH3)3CCl
+(CH3)3CCl| 无水AlCl3 |
 +HCl
+HCl +(CH3)3CCl
+(CH3)3CCl| 无水AlCl3 |
 +HCl
+HCl查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| △ |
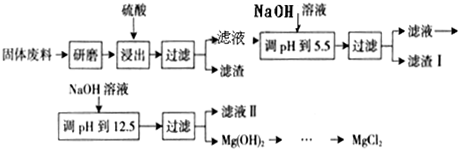
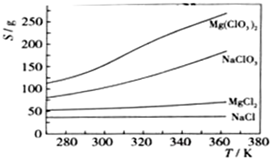
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |
查看答案和解析>>
科目:高中化学 来源:化学(3+2)理科卷东西海最新高考标准模拟试卷 题型:058
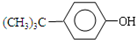
实验室中用浓盐酸与![]() 制
制![]() ,再用
,再用![]() 和
和![]() 反应制少量漂白粉.已知
反应制少量漂白粉.已知![]() 和
和![]() 制漂白粉是放热反应,温度稍高即发生副反应:
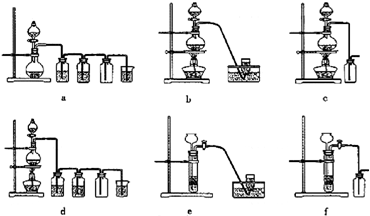
制漂白粉是放热反应,温度稍高即发生副反应:![]() .现有三位同学设计的三套装置如图(U形管中放有玻璃纤维,可使气体顺利通过):
.现有三位同学设计的三套装置如图(U形管中放有玻璃纤维,可使气体顺利通过):

(1)请从以下六方面对上述甲、乙、丙三套装置的优缺点进行评价,将适当的选项序号填于下表内.
a.不易控制反应速率
b.容易控制反应速率
c.有副反应发生
d.可防止副反应发生
e.容易污染环境
f.可防止污染环境

(2)请从甲、乙、丙三装置中,选取合理的组成部分(A、B、C、D、E、F、G),组装一套你认为更完善的实验装置,连接顺序(按气流左到右方向)为________,在此装置及甲、乙、丙三装置中,你认为是否还缺少必要的装置,说明原因________________
查看答案和解析>>
科目:高中化学 来源: 题型:
(1) 实验室制备纯碱(Na2CO3)的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30—35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体。
![]() 四种盐在不同温度下的溶解度(g / 100 g水)表
四种盐在不同温度下的溶解度(g / 100 g水)表
|
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -① | - | - | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
请回答: ![]()
![]()
![]()
![]()
![]() ①反应控制在30—35℃,是因为高于35℃NH4HCO3会分解,低于30℃则反应速率降低 ,为控制此温度范围,通常采取的加热方法为 ;
①反应控制在30—35℃,是因为高于35℃NH4HCO3会分解,低于30℃则反应速率降低 ,为控制此温度范围,通常采取的加热方法为 ;
![]() ②加料完毕,保温30分钟,目的________________________ ;
②加料完毕,保温30分钟,目的________________________ ;
![]() ③静置后只析出NaHCO3晶体的原因__________________________ ;
③静置后只析出NaHCO3晶体的原因__________________________ ;
![]() ④过滤所得母液中含有NaHCO3、NaCl 、NH4Cl、NH4HCO3,加入适当试剂并作进一步处理,使 _________(填化学式)循环使用,回收得到NH4Cl晶体。
④过滤所得母液中含有NaHCO3、NaCl 、NH4Cl、NH4HCO3,加入适当试剂并作进一步处理,使 _________(填化学式)循环使用,回收得到NH4Cl晶体。
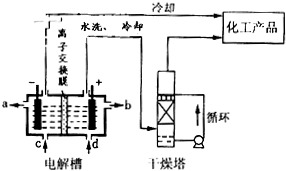
![]() (2)我国科学家侯德榜改革国外的纯碱生产工艺,使其更加先进,被称为侯德榜制碱法,生产流程为:
(2)我国科学家侯德榜改革国外的纯碱生产工艺,使其更加先进,被称为侯德榜制碱法,生产流程为:
![]()
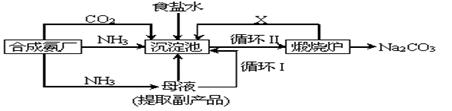
![]() ⑤沉淀池中反应的化学方程式: _______-_______ __ ;
⑤沉淀池中反应的化学方程式: _______-_______ __ ;
![]() ⑥检验产品碳酸钠中是否含有氯化钠的操作方法为: 。
⑥检验产品碳酸钠中是否含有氯化钠的操作方法为: 。
![]() ⑦循环(I)中应该加入或通入物质的化学式为 。
⑦循环(I)中应该加入或通入物质的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com