
| A�� | ��Ӧ�ٵ�����Ӧ�����ȷ�Ӧ | |
| B�� | ��ƽ�⣨I��ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ14��15 | |
| C�� | ��ƽ�⣨I��ʱ��X��ת����Ϊ$\frac{5}{11}$ | |
| D�� | ��ƽ�⣨I����ƽ�⣨II���У�M�ڸ����ұ������е������������ |
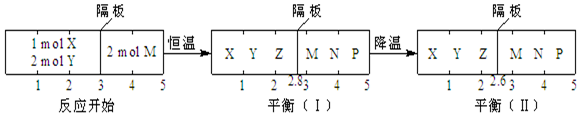
���� A���ӽ��µ���ƽ�⣨I����ƽ�⣨II���ƶ�ʱ��X��Y��Z�������ʵ����仯���·�Ӧ�ƶ��ķ������жϷ�Ӧ�����Ȼ��Ƿ��ȣ�
B�����ݵ���ʱ����Ӧ������������ʵ������䣬ѹǿ������ɷ��ȣ������������������е�ѹǿ��ϵ���жϣ�
C����ͬѹǿ�£��������ʵ���֮�ȵ������֮�ȼ��������������ʵ������������ת���ʣ�
D�������¶ȱ仯��Ӧ�ڵ�ƽ���Ѿ����ƻ���M���������������ȵģ�
��� �⣺A��������ƽ�⣨I����ƽ�⣨II���ƶ���ͬʱX��Y��Z�������ʵ������٣�˵��ƽ�������ƶ�������Ӧ���ȣ���A����
B��ƽ��ʱ���ұ����ʵ������䣬��ͼ���Կ�����ƽ�⣨I��ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ$\frac{2}{2.2}$=$\frac{10}{11}$����B����
C����ƽ�⣨I��ʱ���ұ���������ʵ������䣬��Ϊ2mol����������ѹǿ��ȣ���ƽ��ʱ�����������ʵ���Ϊxmol��$\frac{2}{x}$=$\frac{2.2}{2.8}$�����x=$\frac{28}{11}$�������ʵ�������3mol-$\frac{28}{11}$mol=$\frac{5}{11}$mol�����ڲμӷ�Ӧ��X�����ʵ��������Դ�ƽ�⣨I��ʱ��X��ת����Ϊ$\frac{5}{11}$����C��ȷ��
D����ƽ�⣨I����ƽ�⣨II������ѧ��Ӧ�ڷ����ƶ���M���������������ȵģ���D����
��ѡC��
���� ���⿼�黯ѧƽ���ƶ����⣬Ϊ�߿��������ͺ�Ƶ���㣬���ؿ���ѧ���ķ����������������Ѷ��еȣ�����ע����ұ߷�Ӧ��ϵ�е����ʵ������俼�ǣ�


 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
��
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | H3+�ĵ���ʽΪ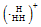 | |
| B�� | H3+�ɽ��з�Ӧ����Һ̬�����γ�H4+��H6+��H8+ | |
| C�� | H3+����Һ̬�����γ�H5+��H7+��H9+ | |
| D�� | H3+�㷺�����ڹ�̬��Һ̬����̬���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HNO3 | B�� | Na2O | C�� | A1C13 | D�� | CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
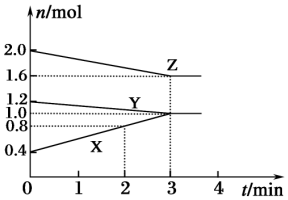 ij�¶�ʱ�����ݻ�Ϊ3L���ܱ������У�X��Y��Z������̬���ʵ����ʵ�����ʱ��仯��������ͼ��ʾ������ͼ�����ݣ��ش��������⣺
ij�¶�ʱ�����ݻ�Ϊ3L���ܱ������У�X��Y��Z������̬���ʵ����ʵ�����ʱ��仯��������ͼ��ʾ������ͼ�����ݣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2CO3 | B�� | NaHCO3 | C�� | Al��OH��3 | D�� | Fe��OH��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������һ���ǽ������ӣ�������һ��ֻ���ǽ���Ԫ�� | |
| B�� | ����������һ��ֻ���������ԣ�û�л�ԭ�� | |
| C�� | ��������������ú�һ���γ����ӻ����� | |
| D�� | �����ͷǽ�������һ���������ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1000mL 3mol/L NaCl��Һ | B�� | 400mL 2.5mol/L MgCl2��Һ | ||
| C�� | 300mL 1mol/L AlCl3��Һ | D�� | 200mL1mol/L ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com