
| A. | Cl2与水的反应:Cl2+H2O═2H++Cl-+ClO- | |
| B. | H2SO4与Ba(OH)2反应:Ba2++SO42-═BaSO4 | |
| C. | 铁溶于足量的稀硝酸:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | 碳酸氢钙溶液跟足量烧碱溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
分析 A.次氯酸为弱电解质,离子方程式中次氯酸不能拆开,需要保留分子式;
B.二者反应生成硫酸钡和水,漏掉了生成水的反应;
C.稀硝酸足量,二者反应生成铁离子,不是亚铁离子;
D.烧碱足量,反应生成碳酸钠、碳酸钙沉淀和水,离子方程式中碳酸根离子有剩余.
解答 解:A.Cl2与水的反应生成的HClO为弱酸,不能拆,正确的离子方程式为:Cl2+H2O?H++Cl-+HClO,故A错误;
B.H2SO4与Ba(OH)2反应生成硫酸钡沉淀和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故B错误;
C.铁溶于足量的稀硝酸反应生成硝酸铁、NO气体和水,正确的离子方程式为:Fe+4H++NO3-═Fe3++NO↑+2H2O,故C错误;
D.碳酸氢钙溶液跟足量烧碱溶液反应生成碳酸钠、碳酸钙沉淀和水,反应的离子方程式为:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入NaOH溶液中 Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 硫化亚铁与稀硫酸反应 FeS+2H+═Fe2++H2S↑ | |
| C. | 硫酸铵和氢氧化钡溶液 Ba2++SO42-═BaSO4↓ | |
| D. | 氢氧化钡与稀硫酸反应 Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

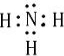 .
.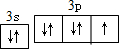 ,其单质在常温下为黄绿色的气体,实验中可以用NaOH溶液吸收,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
,其单质在常温下为黄绿色的气体,实验中可以用NaOH溶液吸收,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝罐可久盛食醋 | |
| B. | 氢氧化铝可作胃酸的中和剂 | |
| C. | 铁表而镀锌可以增强其抗腐蚀性 | |
| D. | 含重金属离子的电镀废液不能随意排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a<c<0 | B. | b>d>0 | C. | 2a=b<0 | D. | 2c=d>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com