
����Ŀ����֪CuSO4��Һ�ֱ���Na2CO3��Һ��Na2S��Һ�ķ�Ӧ���������
(1)CuSO4+Na2CO3
��Ҫ��Cu2++CO32��![]() +H2O��Cu(OH)2��+CO2�� ��Ҫ��Cu2++ CO32����CuCO3��
+H2O��Cu(OH)2��+CO2�� ��Ҫ��Cu2++ CO32����CuCO3��
(2)CuSO4+Na2S
��Ҫ��Cu2++S2����CuS�� ��Ҫ��Cu2++S2��+2H2O��Cu(OH)2��+H2S��
���м������ʵ��ܽ�ȴ�С�ıȽ�������ȷ����( )
A. Cu(OH)2>CuCO3>CuS B. CuS>Cu(OH)2>CuCO3
C. CuS<Cu(OH)2<CuCO3 D. Cu(OH)2<CuCO3<CuS
���𰸡�C
��������������Ӧ�У���������ܽ��ԽС��������ӦԽ��������
CuSO4+Na2CO3����Ҫ����Cu2++CO32��+H2O=Cu��OH��2��+CO2������Ҫ����Cu2++CO32��=CuCO3������˵��Cu��OH��2���ܽ��С��CuCO3���ܽ�ȣ�
CuSO4+Na2S����Ҫ��Cu2++S2��=CuS������Ҫ��Cu2++S2��+2H2O=Cu��OH��2��+H2S������˵��CuS���ܽ��С��Cu��OH��2���ܽ�ȣ����ܽ��CuS��Cu��OH��2��CuCO3����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʯī�缫������й��ʵ�顣
ʵ��һ | ʵ��� | |
װ�� |
|
|
a��d����ֽ������b����죬�ֲ���ɫ��c�������Ա仯 | ����ʯī�缫���������ݲ�����n�������ݲ��������� |
���ж�ʵ������Ľ��ͻ��Ʋⲻ�������ǣ� ��
A. a��d����2H2O+2e-=H2��+2OH- B. b��ʧ���ӣ�����������Ӧ
C. c�������˷�Ӧ��Fe-3e-=Fe3+ D. ����ʵ��һ��ԭ����ʵ�����m��������ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һһ�������Ե��ǣ� ��
A. pH=7����Һ B. �ǵ��������ˮ�γɵ���Һ
C. C(H+)=C(OH-)=10-6 mol/L����Һ D. ��ͼ�ǡ����ȫ��Ӧ���ɵ�������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A. �Ȼ�������ˮ�ܵ����H+��Cl-�������Ȼ��������ӻ�����
B. �⾧������ת��ɵ��������ƻ��˹��ۼ�
C. CH3CH2OH��CH3OCH3��Ϊͬ���칹��
D. ��������þʹ֮�ۻ��˷����ǹ��ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ��һ���ܴ����������( )
A. 0��1 mol��L��1NaOH��Һ��K����Ba2+��Cl����HCO3-
B. 0��1 mol��L��1Na2CO3��Һ��K����NH4+��NO3-��SO42-
C. 0��1 mol��L��1FeCl3��Һ��K����Na����I����SCN��
D. 0��1 mol��L��1HCl����Һ��Ca2����Na����ClO����NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ȡ���ռ�ij�����ʵ��װ�ã���װ�ÿ����ڣ� �� 
A.��Ũ����Ͷ������̷�Ӧ��ȡCl2
B.��Ũ������ͭ��Ӧ��ȡNO2
C.�ù������ƹ����ˮ��Ӧ��ȡO2
D.��Ũ��ˮ����ʯ�ҷ�Ӧ��ȡNH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����t��ʱ��Ag2CrO4���ٺ�ɫ����ˮ�еij����ܽ�ƽ��ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp=4��10-10������˵������ȷ���ǣ� ��

A. ��t��ʱ��Ag2CrO4��KspΪ1��10-8
B. �ڱ�����Һ�м���K2CrO4��ʹ��Һ��Y�㵽Z��
C. ��t��ʱ��Ag2CrO4��s��+2Cl����aq��![]() 2AgCl��s��+CrO42����aq��ƽ�ⳣ��K=6.25��107
2AgCl��s��+CrO42����aq��ƽ�ⳣ��K=6.25��107
D. ��t��ʱ����0.001mol/L AgNO3��Һ�ζ�20mL 0.001mol/L KCl��0.001mol/L��K2CrO4�Ļ����Һ��Cl���ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ�������������( )

A. ͼ�ױ�ʾ��CH3COOH��Һ������CH3COONa�������ҺpH�ı仯
B. ͼ�ұ�ʾ��CH3COOH��Һ�м�ˮʱ��Һ�ĵ����Ա仯����CH3COOH��Һ��pH��a>b
C. ͼ����ʾ�����ܸı仯ѧ��Ӧ���ʱ�
D. ͼ����ʾ����NO2���ݻ���ͬ�ĺ����ܱ������У���ͬ�¶��·ֱ�����Ӧ��2NO2(g)![]() N2O4(g)����ͬʱ�����NO2���������ߣ���÷�Ӧ����H<0
N2O4(g)����ͬʱ�����NO2���������ߣ���÷�Ӧ����H<0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г��õ���������װ�ã�����ʹ�÷�������������
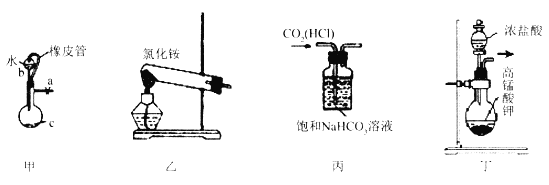
A. װ�üף���Ƥ�ܵ�������ʹˮ˳������
B. װ���ң�ʵ����������ȡ����
C. װ�ñ���ʵ���ҳ�ȥ������̼�л��е��Ȼ�������
D. װ�ö���ʵ����������ȡ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com