
【题目】铝是一种活泼的金属,在高温下能与Fe2O3反应生成Fe和Al2O3。该反应中 (填化学式)是还原剂, (填化学式)是氧化剂, (填化学式)是氧化产物。当反应2mol Fe2O3时,转移了 mol电子。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA阿伏伽德罗常数的值。己知反应
(1)CH4(g)+2O2(g)═CO2(g)+2H2O(l) △H1="a" kJ/mol
(2)CH4(g)+2O2(g)═CO2(g)+2H2O(g) △H2="b" kJ/mol,其它数据如表:
化学键 | C═O | O═O | C-H | O-H |
键能kJ·mol-1 | 798 | x | 413 | 463 |
下列说法正确的是
A. 上表中 x=(1796+b)/2
B. H2O(g)═H2O(l) △S<0,△H═(a-b )kJ/mol
C. 当有4NA个C-H键断裂时,该反应放出热量一定为a kJ
D. 利用反应(1)设计的原电池电解精炼铜时,当负极输出0.2NA个电子时,电解槽的阳极质量一定减轻6.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】-C3H7和-C3H7O取代苯环上的氢原子,形成的有机物中能与金属钠反应的同分异构体有
A. 10种 B. 15种 C. 30种 D. 36种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,可逆反应3X(g)+Y(g)![]() 2Z(g)达到平衡的标志是:
2Z(g)达到平衡的标志是:
A.单位时间内生成3nmolX,同时生成nmolY
B.2v逆(Y)=v正(Z)
C.X、Y、Z的浓度相等
D.X、Y、Z的分子个数比为3:1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是铜与稀硝酸反应的两个实验装置图,请回答下列问题:
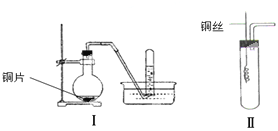
(1)铜与稀硝酸反应的化学方程式_____ _ 。
(2)学生甲用装置Ⅰ探究铜与稀硝酸反应的气体产物。实验过程在烧瓶中观察到有红棕色气体产生,在试管中收集到无色气体。 烧瓶中产生红棕色气体的原因是
(用方程式表示)。
(3)学生乙认为,甲用装置Ⅰ实验,无法说明问题。为了证明并观察到铜与稀硝酸反应的产物为NO,甲设计了如图Ⅱ所示的实验装置,选择下列药品,并按下列实验步骤完成该实验。请你根据他的思路,回答下列问题:
药品:稀硝酸锌粒石灰石固体
步骤:
①检查装置的气密性
②向试管中加入一定量CaCO3固体
③向试管中倒入过量的稀HNO3并迅速盖上带铜丝和导管的橡皮塞
④待反应完全后,将导管插入试管内接近液面
⑤将铜丝插入到溶液中
⑥用注射器的针头穿过橡皮塞并向试管内推入氧气(或空气)
(ⅰ)步骤②目的是 ;
(ⅱ)推入氧气或空气的目的是 ;
(ⅲ)分别将等质量的铜片与等体积均过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出,这可能是Cu2+的浓度差异引起的,你同意这种看法吗?(填“同意”或“不同意”),原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变,且用惰性电极,下列说法不正确的是
A.当电池负极消耗mg气体时,电解池阴极同时有mg气体生成
B.电池的正极反应式为:O2+2H2O+4e-===4OH-
C.电池中c(KOH)不变;电解池中溶液pH变大
D.电解后c(Na2CO3)不变,且溶液中有Na2CO3﹒10H2O晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电石广泛用于生产PVC、维尼纶等,电石与水反应所得残渣——电石渣,主要含Ca(OH)2、CaCO3及少量其他杂质。某工业电石渣的几种回收利用流程如下:
几种物质在水中的溶解度曲线如右图。回答下列问题:
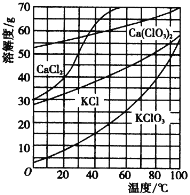
(1)常温氯化
①反应的化学方程式是 。
②提高Cl2转化为Ca(ClO)2的转化率可行的措施有_______(填序号)。
A.加热升高温度 B.适当减缓通入Cl2速率
C.充分搅拌浆料 D.加水使Ca(OH)2完全溶解
③电石渣中的有害杂质CN-与ClO-反应转化为两种无害的气体,每转化1 mol CN-至少需要消耗氧化剂ClO-_______mol。
(2)75 ℃氯化
①生成氯酸钙中氯的化合价为 ,氯化完成后过滤,滤渣的主要成分为______(填化学式)。
②氯酸钙能与KCl反应转化为氯酸钾的原因是 。
(3)有机反应
首先生成氯代乙醇,其结构简式为 ,氯代乙醇再与Ca(OH)2反应生产环氧乙烷。总反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2是形成雾霾天气的原因之一。
(1)重型车辆常在排气管内喷淋尿素[CO(NH2)2]溶液,使NO2转化为无污染物质。采用“喷淋”的目的是 ,反应的活化能 (选填“增大”“减小”“不变”),写出该反应的化学方程式: 。【已知:CO(NH2)2中N呈-3价】
(2)以CO2与NH3为原料可合成化肥尿素。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-l59.5 kJ·mol-1
②NH2CO2NH4(s) =CO(NH2)2(s)+H2O(l) ΔH=-160.5 kJ·mol-1
③H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出CO2与NH3合成尿素和气态水的热化学反应方程式 。
(3)恒温下将1.6 mol NH3和0.8 mol CO2放入容积为8 L的恒容密闭容器中,反应生成NH2CO2NH4(s),下列各项能说明反应达到平衡状态的是 。
a.容器内气体压强保持不变 b.CO2与NH3的速率之比为1∶2
c.NH2CO2NH4(s)质量保持不变 d.容器内温度保持不变
该反应达到平衡时,测得CO2的物质的量浓度为0.05 mol·L-1。则平衡时CO2的转化率α= ;若其他条件不变,移去少量NH2CO2NH4,CO2的转化率 (选填“增大”“减小”“不变”)。

(4)为减少NO2排放,可将NO2转化为NO后通入如右图所示装置,同时补充气体物质A使NO全部转化为NH4NO3,该装置中总化学反应方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com