



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������15�� | B������15�� | C����15�� | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ڱ�״���£�11.2L NH3����5NA������ |
| B��Na2O2��CO2��Ӧ����1molO2ʱ��ת�Ƶ�����Ϊ4NA |
| C��SO2��CO2��NO��NO2���Ǵ�����Ⱦ�ʵ���ж��������β������ |
| D��������Ư�۳���������ˮ�ľ�����ɱ�����������ߵ�����ԭ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ڱ�״���£�33.6LSO3�к��е���ԭ������4.5NA |
| B�����ݾ�Ϊ2.7g������Ʒ�ֱ�Ϊ100mLŨ�Ⱦ�Ϊ2mol��L-1�����������������Һ��ַ�Ӧ��ת�Ƶĵ�������Ϊ0.3 NA |
| C�����³�ѹ�£�agC2H4��C3H6�Ļ���������������õ��Ӷ���ĿΪ3a/14��NA |
| D��6.0g���ʯ�к��еĹ��ۼ���Ϊ2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��25��ʱ��pH��13�İ�ˮ�к���OH������ĿΪ0.1NA |
| B��1 mol Na����ȫ��������Na2O2��ת�Ƶ��ӵ���ĿΪNA |
| C����״���£�2.24 LNO2��ˮ��Ӧ����NO3������ĿΪ0.1NA |
| D��4.0 g H2������������ȫ��Ӧ����NH3����Ӧ�ж��ѹ��ۼ�������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1L 1mol?L-1��NH4Cl��Һ��һ������NA��NH4+ |
| B�����³�ѹ�£�22.4L��ϩ�к����ۼ���Ϊ5 NA |
| C��6.8g���ڵ�KHSO4�к���0.05 NA�������� |
| D��1mol�������lmo1�Ҵ���Ũ��������·�Ӧ������NA��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
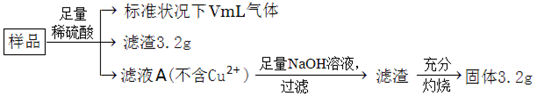
| A����ҺA��������ΪFe2+��H+ |
| B����Ʒ�н���Fe������Ϊ2.14g |
| C����Ʒ��CuO������Ϊ4.0g |
| D��V��448 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1mol Cl2�������þ����Ӧ��ת��2nA������ |
| B�������£�16g CH4����8nA������ |
| C��1L 0.5 mol��L��1Na2SO4��Һ�к���nA��SO42- |
| D�����³�ѹ�£�22.4LCO2����nA��CO2���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com