
����Ŀ����֪ˮ��25����95��ʱ�������ƽ����������ͼ��ʾ��

��1����25��ʱˮ�ĵ���ƽ������ӦΪ_________������A������B��������˵������ ��
��2��25��ʱ����pH=9��NaOH��Һ��pH=4��H2SO4��Һ��ϣ������û����Һ��pH=7����NaOH��Һ��H2SO4��Һ�������Ϊ__________.
��3��95��ʱ����100���pH1=a��ijǿ����Һ��1���pH2=b��ijǿ����Һ��Ϻ���Һ�����ԣ�����ǰ����ǿ���pH1��ǿ���pH2֮��Ӧ����Ĺ�ϵ��_________________.
��4������B��Ӧ�¶��£�pH=2��ijHA��Һ��pH=10��NaOH��Һ�������Ϻ����Һ��pH=5.�������ԭ�� ��
���𰸡�
��1��A��ˮ�ĵ���Ϊ���ȹ��̣��¶�Խ�ͣ�ˮ�����ӻ�ԽС��
��2��10:1��
��3��pH1+pH2=14��a+b=14��
��4������B��Ӧ�¶�Ϊ95������ʱˮ�����ӻ�Ϊ10-12��HAΪ���ᣬHA�к�NaOH��ʣ��϶��HA���������H+��ʹ��Һ��������
��������
�����������1��ˮ�ĵ��������ȹ��̣������¶ȣ�ʹˮ�ĵ���̶������¶�����ʱ���ٽ�ˮ�ĵ��룬ˮ�����ӻ�����ˮ�������ӡ�����������Ũ�ȶ�����ˮ��pH��С������Һ��Ȼ�����ԣ��ʴ�Ϊ��A��ˮ�ĵ��������ȹ��̣��¶�Խ�ͣ�ˮ�����ӻ�ԽС��
��2��25��ʱ���û����Һ��pH=7����Һ�����Լ����ǡ���кͣ���n��OH-��=n��H+������V��NaOH��10-5 molL-1=V��H2SO4��10-4 molL-1����V��NaOH����V��H2SO4��=10��1���ʴ�Ϊ��10��1��
��3��ǿ���pH=a��ǿ���pH=b����95��ʱ����100�����ijǿ����Һ��1�����ijǿ����Һ��ͺ���Һ�����ԣ���n��H+��=n��OH-������100��10-a=1��10b-12��102-a=10b-12����2-a=b-12����a+b=14���ʴ�Ϊ��a+b=14��
��4������B��Ӧ�¶��£�pH=2��HA��Һ��pH=10��ijNaOH��Һ�������Ϻ������Ӻ�����������ǡ�÷�Ӧ���������ǿ�ᣬ������Һ�����ԣ�ʵ������Һ�����ԣ�����Ϊ���ᣬ����ǿ��������ˮ��ʼ��ԣ��кͺ�����Һ�л�ʣ��϶��������ӣ��ɼ��������H+��ʹ��Һ�����ԣ��ʴ�Ϊ������B��Ӧ�¶�Ϊ95������ʱˮ�����ӻ�Ϊ10-12��HAΪ���ᣬHA�к�NaOH��ʣ��϶��HA���������H+��ʹ��Һ�����ԡ�


 ����С����ҵ��ϵ�д�
����С����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������й�ͼ��˵����ȷ���ǣ� ��
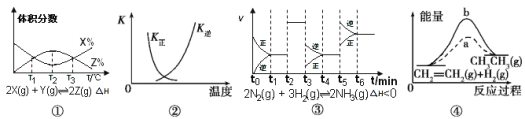
A����ͼ��֪����Ӧ��T1��T3���ﵽƽ�⣬�Ҹ÷�Ӧ�ġ�H��0
B��ͼ�������߱�ʾ��Ӧ2SO2(g)+O2(g) ![]() 2SO3(g),��H<0�����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯
2SO3(g),��H<0�����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯
C����ͼ��֪����Ӧ��t6ʱ��NH3����������t3ʱ��ȡ���ͷ�Ӧ�¶ȵĴ�ʩ
D��ͼ����a��b���߷ֱ��ʾ��ӦCH2= CH2(g)+H2(g) ![]() CH3CH3(g) ��H<0ʹ�ú�δʹ�ô���ʱ, ��Ӧ�����е������仯
CH3CH3(g) ��H<0ʹ�ú�δʹ�ô���ʱ, ��Ӧ�����е������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ij���Ԫ�أ�������ÿ����Ҫ800���˵ĸƣ����в��Ƶ�;����ȷ����
A��������ɹ̫�� B����������ţ�̡�����
C���������ø����Ӻ����ߵ�Ӳˮ D����������ά����C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У����÷�Һ©�����з�����ǣ� ��
A.�ƾ���ˮ
B.������Ȼ�̼
C.ˮ�����Ȼ�̼
D.���ͺ�ֲ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֤������û����ȫˮ�����Լ���
A�����Ƶ�������ͭ B����ˮ C��������Һ D���⻯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в����в���ȷ���ǣ� ��
A.����ʱ����������������ֽ��һ�߽Ӵ�
B.����ʱ��©���¶˽����ձ��ڱ�
C.�����Թ�������ʱ���Թܵײ���ƾ�������Ӵ�
D.���Թ��еμ�Һ��ʱ����ͷ�ιܽ����Թ��ڱ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݲ��ֶ�����Ԫ�ص���Ϣ�ش����⡣
Ԫ�� | Ԫ����Ϣ |
A | ��3���ڢ�A�� |
B | ����������������3�� |
C | ԭ��������11 |
D | D3+��Ne�ĵ�������ͬ |
��1��A��B��Ԫ�ط���Ϊ________��________,C��D��Ԫ������Ϊ________��________��
��2��д��B��C�ij��������ڼ���ʱ�ķ�Ӧ����ʽ:________��
��3����ԭ�ӽṹ�ĽǶȷ���,Aԭ����Bԭ�ӵ�________��ͬ,Cԭ����Dԭ�ӵ�________��ͬ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ͬϵ�����ʽΪC8H10���������ϵ���ԭ�ӱ�±ԭ��ȡ�������ɵ�һ±����������ͬ���칹�壬��ñ���ͬϵ�������(����)
A. 4�� B. 3�� C. 2�� D. 1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��a��b��c��d��e��f��gΪ�����ɶ�����Ԫ�ع��ɵ����ӣ����Ƕ�����10�����ӣ���ṹ�ص����£�
���Ӵ��� | a | b | c | d | e | f | g |
ԭ�Ӻ��� | ���� | ���� | ˫�� | ��� | ���� | ��� | ��� |
�����(����) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
����b�����Ӱ뾶����e�����Ӱ뾶��d���ɼ��Լ����ɵ���ԭ�ӷ��ӣ�c��f��һ���������γ�һ��g���Ӻ�һ��d���ӣ���д����
(1)a���ӵ�ԭ�ӽṹʾ��ͼ___________
(2)b��e��ӦԪ�ص�����������Ӧˮ����ļ���ǿ���Ƚ�Ϊ___��_____ (�û�ѧʽ��ʾ)��
(3)d��һ�ֺ��м��Լ�˫��18���ӷ��ӷ�Ӧ�Ļ�ѧ����ʽΪ ______��
(4)g��һ�ֺ��зǼ��Լ�˫��18���ӷ��ӷ�Ӧ�Ļ�ѧ����ʽΪ__________
������Ӧ�У����ѻ�ѧ����__________��д���Ļ�ѧ����________������Ӽ����������Լ��������Ǽ��Լ��������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com