
����Ŀ��ͼ��A��B��C��D��E��F��G��Ϊ�л������������ͼ��ʾת����ϵ�ش��������⣺

(1)D�Ļ�ѧ������___________________��
(2)��Ӧ�۵Ļ�ѧ����ʽ��______________________________________________________��
(3)B�ķ���ʽ��_________��A�Ľṹ��ʽ��_________����Ӧ�ٵķ�Ӧ������_________��
(4)������������������B��ͬ���칹�壨������B����_________�֡�
����B����ͬ�������ұ�����ֻ������ȡ���� �ڲ���![]() ��Һ������ɫ��Ӧ
��Һ������ɫ��Ӧ
д����������һ��ͬ���칹��Ľṹ��ʽ��_______________��
(5)��Ӧ�ܵĻ�ѧ����ʽ��_________________________________________________________________��G����Ҫ�Ĺ�ҵԭ�ϣ��û�ѧ����ʽ��ʾG�γɸ߾���ķ�Ӧ��__________________________��
���𰸡��Ҵ� ![]()
![]()
![]() ˮ�ⷴӦ 11
ˮ�ⷴӦ 11 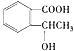 ������������Ҳ�ɣ�
������������Ҳ�ɣ� ![]()
![]()
��������
B��Ũ�����������������E����E�Ľṹ��֪��B����������Ӧ����E����BΪ![]() ��D�ķ���ʽΪC2H6O��һ�������¿�������C2H4����DΪCH3CH2OH��GΪCH2=CH2��C��CH3CH2OH��Ũ���ᡢ��������������F�����F�ķ���ʽC4H8O2��֪������F�ķ�ӦΪ������Ӧ����CΪCH3COOH��FΪCH3COOCH2CH3��A����������ˮ��Һ�����������·���ˮ�ⷴӦ���ữ�õ�B��C��D����AΪ
��D�ķ���ʽΪC2H6O��һ�������¿�������C2H4����DΪCH3CH2OH��GΪCH2=CH2��C��CH3CH2OH��Ũ���ᡢ��������������F�����F�ķ���ʽC4H8O2��֪������F�ķ�ӦΪ������Ӧ����CΪCH3COOH��FΪCH3COOCH2CH3��A����������ˮ��Һ�����������·���ˮ�ⷴӦ���ữ�õ�B��C��D����AΪ![]() ��
��
��1��D�ķ���ʽΪC2H6O��һ�������¿�������C2H4����DΪCH3CH2OH����ѧ����Ϊ�Ҵ����ʴ�Ϊ���Ҵ���
��2����Ӧ����CH3COOH��CH3CH2OH����������Ӧ����������������Ӧ����ʽΪ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��3��B��Ũ�����������������E����E�Ľṹ��֪��B����������Ӧ����E��BΪ![]() ��D�ķ���ʽΪC2H6O��AΪ
��D�ķ���ʽΪC2H6O��AΪ![]() ��A����������ˮ��Һ�����������·���ˮ�ⷴӦ���ữ�õ�B��C��D����Ӧ�ٵķ�Ӧ������ˮ�ⷴӦ���ʴ�Ϊ��
��A����������ˮ��Һ�����������·���ˮ�ⷴӦ���ữ�õ�B��C��D����Ӧ�ٵķ�Ӧ������ˮ�ⷴӦ���ʴ�Ϊ�� ![]() ��
�� ![]() ��ˮ�ⷴӦ��
��ˮ�ⷴӦ��
��4��������������������B��ͬ���칹�壨������B������B����ͬ�������ұ�����ֻ������ȡ���� �ڲ���![]() ��Һ������ɫ��Ӧ��û�з��ǻ���
��Һ������ɫ��Ӧ��û�з��ǻ���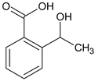 ���ڡ��䡢��3�֣���
���ڡ��䡢��3�֣���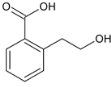 ���ڡ��䡢��3�֣���
���ڡ��䡢��3�֣���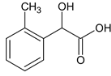 ���ڡ��䡢��3�֣���
���ڡ��䡢��3�֣��� ���䡢��2�֣���11�֣��ʴ�Ϊ��11��
���䡢��2�֣���11�֣��ʴ�Ϊ��11�� ������������Ҳ�ɣ���
������������Ҳ�ɣ���
��5��DΪ�Ҵ�����Ӧ�����Ҵ�������ȥ��Ӧ������ϩ����ѧ����ʽ��![]() ��G����Ҫ�Ĺ�ҵԭ�ϣ�GΪCH2=CH2���γɸ߾���ķ�Ӧ��
��G����Ҫ�Ĺ�ҵԭ�ϣ�GΪCH2=CH2���γɸ߾���ķ�Ӧ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ NH4Cl�����ᡢNaClO2 Ϊԭ���Ʊ� ClO2 �Ĺ�������ͼ��ʾ������˵������ȷ����
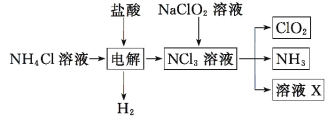
A.X �д������ڵ��������� Cl-�� OH-B.NCl3 �ļ��DZ� CH4 �ļ��Ǵ�
C.NaClO2 ��� ClO2 ������������ӦD.��ȡ 3 mol ClO2 ������Ҫ 0.5mol NH4Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������NaOH����Һ������ȫ��Ӧ�ɵ�3���л�����ǣ� ��
A��CH3��CHCl��CH2��CH3
B��
C��CH3��C��CH3��Cl��CH2��CH3
D��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.ij����ˮ�к�KCN����Ũ��Ϊ0.01 mol��L��1���������������������������·�Ӧ(��������N���ϼ۾�Ϊ��3��)��
KCN��2KOH��Cl2===KOCN��2KCl��H2O
��1��������Ӧ�б�������Ԫ����________(��Ԫ�ط��ű�ʾ)��
��2��Ͷ�����Һ�ȣ��ɽ������ν�һ������Ϊ����������ƽ���л�ѧ����ʽ��______________
______KOCN��______Cl2��______![]() ===______K2CO3��______N2��______KCl��______
===______K2CO3��______N2��______KCl��______![]()
��3������10 L��KCN��Ũ��Ϊ0.01 mol��L��1�ķ�ˮ��KCN������ȥ��������Ҫ����________ mol��
��.ijʵ��С��Ϊ�˲ⶨ(3)����Һ����Cl2�ĺ���������Na2S2O3����Һ���ж����ⶨ��
��4����ʵ��������480 mLһ��Ũ�ȵ�Na2S2O3��Һ�����Ƹ���Һ���貣���������ձ�����Ͳ������������ͷ�ι��⣬����________��
��5��Na2S2O3��ԭ�Խ�ǿ������Һ���ױ�Cl2������SO![]() �����Na2S2O3���������ȼ����÷�Ӧ�����ӷ���ʽΪ_________________��
�����Na2S2O3���������ȼ����÷�Ӧ�����ӷ���ʽΪ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E����Ԫ�أ����ǵĺ˵�������������Ҷ�С��20������C��E�ǽ���Ԫ�أ�A��E��ͬһ�壬����ԭ�ӵ����������Ų�Ϊns1��B��DҲ��ͬһ�壬����ԭ��������p�ܼ���������s�ܼ���������������Cԭ����������������Dԭ��������ϵ�������һ�롣��ش��������⣺
(1)д��CԪ�ػ�̬ԭ�ӵĵ����Ų�ʽ��_________��
(2)�ù����ʾʽ��ʾDԪ��ԭ�ӵļ۵��ӹ��ͣ�________��
(3)д��E���ӵĽṹʾ��ͼ��_________��
(4)Ԫ��B��D�ĵ縺�ԵĴ�С��ϵ��B________D��C��E�ĵ�һ�����ܵĴ�С��ϵ��C________E��(��>��<����)
(5)��������Ԫ����ɵ�һ�ֻ�������(д��ѧʽ)________��д�������ʵ�һ����Ҫ��;��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��L-�����һ���л������ʽΪC9H11O4N��������������ɭ�������ƣ���ṹ��ʽΪ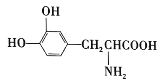 �����й���L-��͵���������ȷ���ǣ� ��
�����й���L-��͵���������ȷ���ǣ� ��
A.��������-�����ᣬ�Ⱦ������ԣ��־��м���
B.������FeCl3��Һ������ɫ��Ӧ
C.������ͨ�������Ӽ������γɷ���ʽΪC18H18O6N2�Ļ�����û���������3����Ԫ��
D.�������ᷴӦ����Ӧ�������ʵ�����L-���������ĵ�NaOH��HC1�����ʵ���֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���1L0.1mol��L-1��CH3COOH��Һ�д������µ���ƽ�⣺CH3COOH![]() CH3COO-+H+�����ڸ�ƽ�⣬����������ȷ���ǣ� ��
CH3COO-+H+�����ڸ�ƽ�⣬����������ȷ���ǣ� ��
A.����ˮʱ��ƽ�����淴Ӧ�����ƶ�
B.��������NaOH���壬ƽ��������Ӧ�����ƶ�
C.��������0.1mol��L-1HCl��Һ����Һ��c(H+)��С
D.��������CH3COONa���壬ƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������������Ӧ���Ȼ�ѧ����ʽ��25�桢101kPa����
��C4H10��g��+![]() O2��g���T 4CO2��g��+5H2O��l������H=-2 878kJ/mol
O2��g���T 4CO2��g��+5H2O��l������H=-2 878kJ/mol
��C4H10��g��+![]() O2��g���T 4CO2��g��+5H2O��g������H=-2 658kJ/mol
O2��g���T 4CO2��g��+5H2O��g������H=-2 658kJ/mol
��C4H10��g��+![]() O2��g���T 4CO��g��+5H2O��l������H=-1 746kJ/mol
O2��g���T 4CO��g��+5H2O��l������H=-1 746kJ/mol
��C4H10��g��+![]() O2��g���T 4CO��g��+5H2O��g������H=-1 526kJ/mol
O2��g���T 4CO��g��+5H2O��g������H=-1 526kJ/mol
�ɴ��жϣ��������ȼ����Ϊ��������
A.2878kJ/molB.2658kJ/molC.1746kJ/molD.1526kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���߷��Ӳ�������66�������õĿ�����ԡ����ԡ���ȼ���Ժ���ȼ����Ե���ص㣬��˹㷺Ӧ���������������ȹ�ҵ�С���������������66��һЩ;����
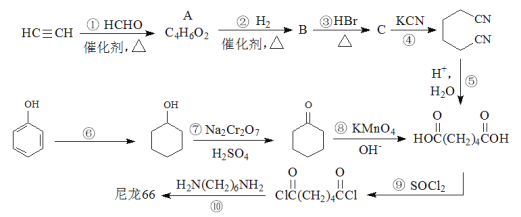
��1��A�Ľṹ��ʽΪ_____________��
��2��B�й����ŵ�������_____________��
��3����Ӧ��~���У����ڼӳɷ�Ӧ����_______����Ӧ��~���У�����������Ӧ����_______��
��4����д����Ӧ�Ļ�ѧ����ʽ_____________��
��5���߷��Ӳ�������66�к���![]() �ṹƬ�Σ���д����Ӧ��Ļ�ѧ����ʽ_____________��
�ṹƬ�Σ���д����Ӧ��Ļ�ѧ����ʽ_____________��
��6��ij�ۺ���K�ĵ�����A��Ϊͬ���칹�壬�õ���˴Ź��������������壬�����֮��Ϊ1:2:3��������NaHCO3��Һ��Ӧ����ۺ���K�Ľṹ��ʽ��_____________��
��7�������ᣨ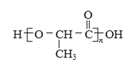 ����һ������ɽ�����ϣ���֪�ʻ�������ɷ�������
����һ������ɽ�����ϣ���֪�ʻ�������ɷ�������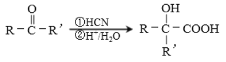 ��Ӧ�� ��R��������������Hԭ�ӣ����úϳ�·��ͼ��ʾ���Ҵ��Ʊ�������Ĺ��̡�_______________
��Ӧ�� ��R��������������Hԭ�ӣ����úϳ�·��ͼ��ʾ���Ҵ��Ʊ�������Ĺ��̡�_______________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com