
(14分)
Ⅰ、实验室常用以下方法制取氯气:MnO2+ 4HCl(浓)  MnCl2+Cl2↑
+ 2H2O,
MnCl2+Cl2↑
+ 2H2O,
(1)用双线桥标出电子转移方向和数目。(在答题纸上标)
(2)在标准状况下生成的Cl2为11.2L时,参加反应的HCl的物质的量为 ,
被氧化HCl的质量为 。
Ⅱ、科学家发现,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒。这是因为
对人体无害的+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化
合物。通过以上信息填空:
(1)维生素C具有 (填氧化性或还原性)。
(2)上述过程中+5价砷类物质作为 (填氧化剂或还原剂),+5价砷元素发生
反应(填氧化或还原);2mol +5价砷完全转化为 +3价砷,共转移 个
电子(用NA表示阿伏加德罗常数)。
(每空2分,共14分)
Ⅰ、(1)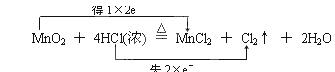 (2)2mol,36.5g。
(2)2mol,36.5g。
Ⅱ、(1) 还原性 (2)氧化剂 ; 还原 ;4NA
【解析】
试题分析:Ⅰ、(1)根据反应的方程式可知,盐酸中氯元素的化合价从-1价升高到0价,失去1个电子。而二氧化锰中Mn元素的化合价从+4价降低到+2价,得到2个电子,所以根据电子到得失守恒可知,正确的表示应该是 。
。
(2)氯气的物质的量是11.2L÷22.4L/mol=0.5mol,则根据反应的化学方程式可知,参加反应的氯化氢是0.5mol×4=2mol。其中被氧化的氯化氢是1mol,质量是36.5g。
Ⅱ、(1)+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化,这说明砷元素得到电子,所以维生素C失去电子,具有还原性。
(2)As元素的化合价从+5价降低到+3价,得到2个电子,做氧化剂,则+5价砷元素发生还原反应。2mol +5价砷完全转化为 +3价砷,得到4mol电子,则共转移4NA个电子。
考点:考查氧化还原反应的表示、计算以及有关判断
点评:该题是基础性试题的考查,也是高考中的常见考点,难度不大。试题放热关键是熟练掌握氧化还原反应的有关概念,判断的依据,然后再结合题意灵活分析即可。该题有利于培养学生分析问题、解决问题的能力。


科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省济宁市鱼台一中高一3月月考化学试卷(带解析) 题型:填空题
(14分)
Ⅰ、实验室常用以下方法制取氯气:MnO2+ 4HCl(浓)  MnCl2+Cl2↑ + 2H2O,
MnCl2+Cl2↑ + 2H2O,
(1)用双线桥标出电子转移方向和数目。(在答题纸上标)
(2)在标准状况下生成的Cl2为11.2L时,参加反应的HCl的物质的量为 ,
被氧化HCl的质量为 。
Ⅱ、科学家发现,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒。这是因为
对人体无害的+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化
合物。通过以上信息填空:
(1)维生素C具有 (填氧化性或还原性)。
(2)上述过程中+5价砷类物质作为 (填氧化剂或还原剂),+5价砷元素发生
反应(填氧化或还原);2mol +5价砷完全转化为 +3价砷,共转移 个
电子(用NA表示阿伏加德罗常数)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省厦门一中高一上学期期中化学试卷 题型:填空题
Ⅰ、实验室常用以下方法制取氯气:MnO2+ 4HCl(浓)  MnCl2+
MnCl2+  Cl2↑+ 2H2O,
Cl2↑+ 2H2O,
(1)用双线桥标出电子转移方向和数目。(在答题卷上标)
(2)在标准状况下生成的Cl2为11.2L时,参加反应的HCl的物质的量为 ,被氧化HCl的质量为 。
Ⅱ、科学家发现,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒。这是因为对人体无害的+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化合物。通过以上信息填空:
(1)维生素C具有 (填氧化性或还原性)。
(2)上述过程中+5价砷类物质作为 (填氧化剂或还原剂),+5价砷元素发生 反应(填氧化或还原);2mol +5价砷完全转化为 +3价砷,共转移 个电子(用NA表示阿伏加德罗常数)。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年福建省厦门一中高一(上)期中化学试卷(解析版) 题型:解答题
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com