
利用铝热反应焊接钢轨的原理是2Al+Fe2O3 2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。
2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。
样品处理:将褐色硬块处理成粉末状。
(1)研究小组首先取少量粉末加入 溶液中,发现粉末部分溶解,但没有气泡产生,实验结论是:粉末中含有Al2O3而没有Al。
(2)根据以述实验判断该褐色硬块的组成基本确定为Fe、Fe2O3、Al2O3。
提出假设:
假设1:固体粉末中除Al2O3外还有Fe;
假设2:固体粉末中除Al2O3外还有 ;
假设3:固体粉末中除Al2O3外还有Fe和Fe2O3。
实验实施:
(3)请以上述粉末为样品,验证其组成。限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3mol/LNaOH、3mol/LHCl、3mol/LHNO3、3mol/LCuSO4、0.01mol/LKMnO4、蒸馏水。
根据你设计的实验方案,叙述实验操作、预期现象和结论。
|
实验操作 |
预期现象和结论 |
|
|
|
|
步骤2:将步骤1的滤渣转移到烧杯B中,加入足量 ,充分搅拌,过滤,洗涤。 |
有红色固体生成,说明粉末中含有
。 |
|
步骤3:将步骤2的滤渣转移到烧杯C中,
。 |
, 说明粉末中含有Fe2O3。(1分) |
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| 实验操作 | 预期现象和结论 |
| 步骤1: | 粉末减少,说明粉末国可能含有Al2O3 粉末减少,说明粉末国可能含有Al2O3 |
| 步骤2: | 有白色沉淀产生然后沉淀又溶解,说明粉末中含有Al2O3 有白色沉淀产生然后沉淀又溶解,说明粉末中含有Al2O3 |
| 步骤3: | 有红色固体生成,说明粉末中含有Fe 有红色固体生成,说明粉末中含有Fe |
| 步骤4: | 固体部分溶解,溶液变血红色,说明粉末中含有Fe2O3 固体部分溶解,溶液变血红色,说明粉末中含有Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
利用铝热反应焊接钢轨的原理是2Al+Fe2O3![]() 2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。
2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。
样品处理:将褐色硬块处理成粉末状。
(1)研究小组首先取少量粉末加入 溶液中,发现粉末部分溶解,但没有气泡产生,实验结论是:粉末中含有Al2O3而没有Al。
(2)根据以述实验判断该褐色硬块的组成基本确定为Fe、Fe2O3、Al2O3。
提出假设:
假设1:固体粉末中除Al2O3外还有Fe;
假设2:固体粉末中除Al2O3外还有 ;
假设3:固体粉末中除Al2O3外还有Fe和Fe2O3。
实验实施:
(3)请以上述粉末为样品,验证其组成。限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3mol/LNaOH、3mol/LHCl、3mol/LHNO3、3mol/LCuSO4、0.01mol/LKMnO4、蒸馏水。
根据你设计的实验方案,叙述实验操作、预期现象和结论。
| 实验操作 | 预期现象和结论 |
|
|
|
| 步骤2:将步骤1的滤渣转移到烧杯B中,加入足量 ,充分搅拌,过滤,洗涤。 | 有红色固体生成,说明粉末中含有
。 |
| 步骤3:将步骤2的滤渣转移到烧杯C中,
。 |
, 说明粉末中含有Fe2O3。(1分) |
查看答案和解析>>
科目:高中化学 来源:2014届浙江台州六校高二上期期中文化学试卷(解析版) 题型:选择题
高铁的快速发展方便了人们的出行。工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:2Al+Fe2O3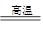 Al2O3+2Fe,其中Fe2O3是
Al2O3+2Fe,其中Fe2O3是
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com