
硫的氧化物、氮的氧化物和一氧化碳是大气的主要污染物,防止和治理环境污染是当前环保工作的重要研究内容之一。
(1)有下列反应:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
S(g)与O2(g)反应生成SO2(g)的热化学方程式为 。
![]() (2)一定条件下,2SO2(g)+O2(g) 2SO3(g),向2L密闭容器中通入
(2)一定条件下,2SO2(g)+O2(g) 2SO3(g),向2L密闭容器中通入
2 mol SO2(g)、1 mol O2(g)和0.2 mol SO3(g),2 min后反应达到平衡时,测得SO2的物质的量为1 mol,恒温下,若往容器中再加入2 mol SO2(g),则重新达到平衡时SO2的总转化率 50%(选填“>","<"或"=")。
![]() (3)在一密闭容器中发生反应2NO2 2NO+O2,反应过程中NO2的浓度随时间变化
(3)在一密闭容器中发生反应2NO2 2NO+O2,反应过程中NO2的浓度随时间变化
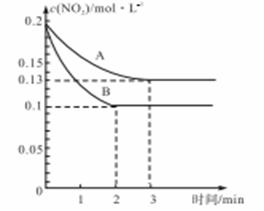 的情报况如下图所示,请回答:
的情报况如下图所示,请回答:
①依曲线A,反应在前3min内氧气的平均反应速率为 ;
②若曲线A、B分别表示的是该反应在保持其他条件不变时,只改变其中一个外界条件时的变化情况,则此条件是
(填“浓度”、“压强”、“温度”或“催化剂”)
![]() (4)工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g) CH3OH(g)
(4)工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g) CH3OH(g)
某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.l mol·L -1。
①该反应的平衡常数K= :
②在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有
关说法正确的是 (填序号)。
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2) / n(CH3OH)增大
科目:高中化学 来源: 题型:
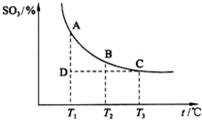 (2013?潍坊模拟)如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.
(2013?潍坊模拟)如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.| 3 |
| 2 |
| H | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间 | 开始 | 8h后 | 16h后 | 24h后 | 32h后 | 40h后 | 48h后 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
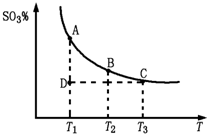 (2010?泰安二模)研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.
(2010?泰安二模)研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.| 3 | 2 |
查看答案和解析>>
科目:高中化学 来源:陕西省模拟题 题型:填空题
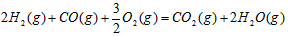
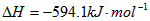 。请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式_____________________;
。请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式_____________________;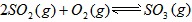 ,平衡混合体系中SO3的百分含量和温度的关系如图所示。 根据图示回答下列问题:
,平衡混合体系中SO3的百分含量和温度的关系如图所示。 根据图示回答下列问题: 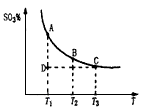
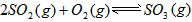 的△H_______0(填“>”或“<”);
的△H_______0(填“>”或“<”); 查看答案和解析>>
科目:高中化学 来源:陕西省模拟题 题型:填空题
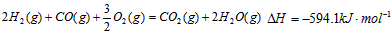 。请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式____________________;
。请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式____________________; 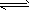 2SO3(g)平衡混合体系中SO3的百分含量和温度的关系如图所示。根据图示回答下列问题
2SO3(g)平衡混合体系中SO3的百分含量和温度的关系如图所示。根据图示回答下列问题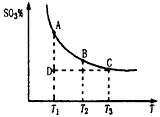
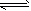 2SO3(g)的△H_______0(填“>”或“<”);
2SO3(g)的△H_______0(填“>”或“<”);查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com