

 ;I的分子式是C8H6O3.
;I的分子式是C8H6O3.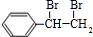 +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$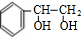 +2NaBr;反应类型属于水解反应.
+2NaBr;反应类型属于水解反应.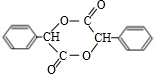 .
. 或
或 .
.分析 苯乙烯发生聚合反应生成F,则F的结构简式为 ,苯乙烯与溴发生加成反应生成E,故E为
,苯乙烯与溴发生加成反应生成E,故E为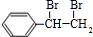 ,由K的结构简式可知,J发生缩聚反应生成K,故J为
,由K的结构简式可知,J发生缩聚反应生成K,故J为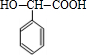 ,E转化得到G,G氧化生成H,H氧化生成I,I与氢气发生加成反应生成J,故G为醇,则G为
,E转化得到G,G氧化生成H,H氧化生成I,I与氢气发生加成反应生成J,故G为醇,则G为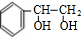 ,H为
,H为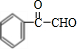 ,I为
,I为 ,据此解答.
,据此解答.
解答 解:苯乙烯发生聚合反应生成F,则F的结构简式为 ,苯乙烯与溴发生加成反应生成E,故E为
,苯乙烯与溴发生加成反应生成E,故E为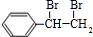 ,由K的结构简式可知,J发生缩聚反应生成K,故J为
,由K的结构简式可知,J发生缩聚反应生成K,故J为 ,E转化得到G,G氧化生成H,H氧化生成I,I与氢气发生加成反应生成J,故G为醇,则G为
,E转化得到G,G氧化生成H,H氧化生成I,I与氢气发生加成反应生成J,故G为醇,则G为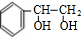 ,H为
,H为 ,I为
,I为 .
.
(1)由上述分析可知,J为 ,含有羟基、羧基,由K的结构简式可知,K中含有酯基,结构简式为-COO-,
,含有羟基、羧基,由K的结构简式可知,K中含有酯基,结构简式为-COO-,
故答案为:羟基、羧基;-COO-;
(2)由上述分析可知,聚合物F的结构简式为 ,I为
,I为 ,分子式是C8H6O3,
,分子式是C8H6O3,
故答案为: ;C8H6O3;
;C8H6O3;
(3)E转化为G的化学方程式是: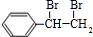 +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$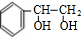 +2NaBr,属于水解反应,
+2NaBr,属于水解反应,
故答案为: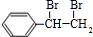 +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$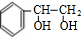 +2NaBr;水解反应;
+2NaBr;水解反应;
(4)在一定条件下,两分子 能脱去两分子水形成一种六元环状化合物,该化合物的结构简式 为:
能脱去两分子水形成一种六元环状化合物,该化合物的结构简式 为: ,
,
故答案为: ;
;
(5) 的一种符合下列条件的同分异构体X:
的一种符合下列条件的同分异构体X:
①.X与FeCl3溶液反应显色,说明含有酚羟基;
②X分子中氢原子核磁共振氢谱有4个峰,可以是苯环上含有2个取代基,另外侧链为-OOCCH3或-COOCH3,且处于对位位置,故符合条件的X的结构简式为: 或
或
故答案为: 或
或 .
.
点评 本题考查有机物的推断与合成,涉及烯烃、卤代烃、醇、醛、羧酸的性质等,掌握官能团的性质是关键,(5)中限制条件同分异构体的书写,为易错点,注意根据题目信息确定含有的官能团.


科目:高中化学 来源: 题型:选择题
| A. |  如图的键线式表示烃的名称为:3-甲基-4-乙基-7-甲基辛烷 | |
| B. | 符合分子式为C3H8O的醇有三种不同的结构 | |
| C. | 乙烯在一定条件下能发生加成反应,加聚反应,被酸化高锰酸钾溶液氧化,也能在一定条件下被氧气氧化成乙酸 | |
| D. |  治疗疟疾的青蒿素(如图),分子式是C15H20O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1>0 | B. | △H2>0 | C. | △H2<△H3 | D. | △H5=2△H4+△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3对 | B. | 4对 | C. | 5对 | D. | 6对 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.05 mol•L-1 Fe2(SO4)3溶液中含Fe3+数目为0.1NA | |
| B. | 标准状况下,22.4 L甲苯中含C-H数目为8NA | |
| C. | 常温常压下,3.2 g O2和O3混合物中,氧原子的数目为0.2NA | |
| D. | 0.1 mol Na2O2与足量CO2反应时,转移的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
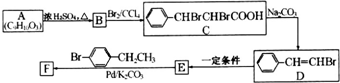
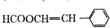 (写结构简式).
(写结构简式).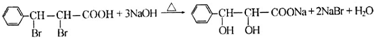
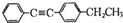 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 易失去电子的物质 | B. | 原子核外有10个电子的微粒 | ||
| C. | 原子的最外层只有1个电子的元素 | D. | 原子核内有12个质子的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
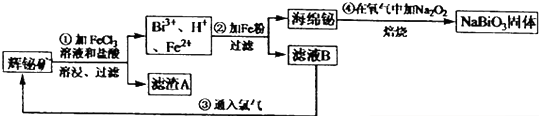
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com