
| A. | CO32ˉ | B. | OHˉ | C. | Fe2+ | D. | Al3+ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 5.2 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;名称是环己烷.
;名称是环己烷.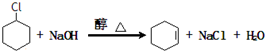 .
. +Br2→
+Br2→ .
. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O.
+2NaBr+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | M的分子式为C12H12O5 | |
| B. | M只能与溴水发生加成反应 | |
| C. | 1mol M最多可和5mol H2发生加成反应 | |
| D. | 1molM最多可消耗3molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水的离子积Kw、随温度变化而变化,在稀盐酸中数值会变大 | |
| B. | 在纯水中加入硫酸会抑制水的电离,加醋酸会促进水的电离 | |
| C. | 向水中加入NaHSO4溶液,抑制水的电离,溶液呈酸性 | |
| D. | 向水中加入NH4Cl溶液,促进水的电离,溶液呈碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com