
| 试剂 | 酚酞试液、CCl4、无水酒精、KSCN溶液 | ||
| 方案 | 操作步骤 | 实验现象 | 结论 |
| 1 | 取所述黄色溶液于试管中,滴加KSCN溶液并振荡 | 溶液变红色 | 反应①所致 |
| 2 | 取所述黄色溶液于试管中,滴加CCl4并振荡 | 溶液分上下两层,上层为黄色、下层为无色 | |
分析 (1)①根据发生氧化还原反应生成Fe3+及Fe3+在水中的颜色来猜想;
②根据溴水的颜色来进行猜想;
(2)利用Fe3+的检验及萃取来进行实验的设计,Fe3+遇KSCN溶液变为红色,溴易溶于四氯化碳中,且四氯化碳与水不溶;
(3)由氧化性Br2>Fe3+,则氯化亚铁溶液中加入1~2滴溴水发生氧化还原反应生成Fe3+;
(4)I.还原性强的离子先被氧化;
Ⅱ.根据电子守恒进行计算.
解答 解:(1)①氧化性:Cl2>Fe3+,则发生2Fe2++Cl2=2Fe3++2Cl-,生成Fe3+且Fe3+在水中为黄色,溶液呈黄色是因为含有Fe3+所致,
②因溴水的颜色为黄色,发生2Br-+Cl2=Br2+2Cl-,则溶液呈黄色是因为含有Br2所致,根据溴水的颜色来进行猜想;
故答案为:2Fe2++Cl2=2Fe3++2Cl-;2Br-+Cl2=Br2+2Cl-;
(2)因Fe3+遇KSCN溶液变为红色,溴易溶于四氯化碳中,且四氯化碳与水不溶,且Fe2+的还原性比Br-强,若溴离子被氧化,溴单质溶解于四氯化碳中,显示橙红色,水和四氯化碳是互不相溶的,三价铁溶解在水中,显示黄色,所以产生的现象是:溶液分上下两层,上层为黄色、下层为无色可知①成立,
故答案为:
| 方案 | 操作步骤 | 实验现象 | 结论 |
| 1 | KSCN溶液 | ① | |
| 2 | CCl4 | 溶液分上下两层,上层为黄色、下层为无色 |
点评 本题考查性质实验方案的设计,为高频考点,涉及氧化还原反应及氧化性、还原性的比较、实验设计等,侧重分析与实验能力的考查,注意物质的性质及氧化还原反应中电子守恒应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
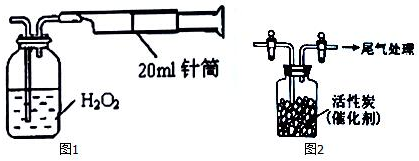
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
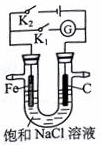
| A. | K1闭合,向铁棒附近滴入K3[Fe(CN)6]溶液,立即有血红色出现 | |
| B. | K2闭合,电流方向由石墨棒经导线流向铁棒 | |
| C. | K2闭合,碳棒上发生还原反应,会生成黄绿色气体 | |
| D. | 将U型管支管封闭并闭合K1一段时间后,U型管中右侧液面会高于左侧液面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
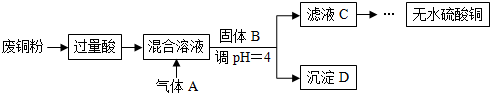
| A. | “过量酸”不适合用硝酸或浓硫酸,固体B可以用CuO、Cu(OH)2或Cu2(OH)2CO3 | |
| B. | 通入的气体A可以是O2或Cl2 | |
| C. | 通入气体A之前的混合溶液中存在的阳离子是:Fe2+、Cu2+、H+ | |
| D. | 将从溶液中得到的硫酸铜晶体在空气中加热,可制得无水硫酸铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
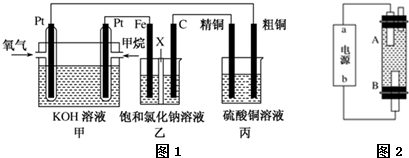
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
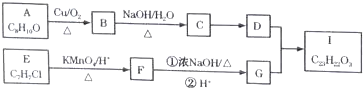
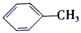 $→_{△}^{KMnO_{4}/H+}$
$→_{△}^{KMnO_{4}/H+}$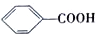
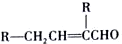
 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com