
| A. | 在水溶液里或熔融状态下能够导电的物质叫做电解质 | |
| B. | 微粒直径在10-9 m-10-7m之间的分散系为胶体 | |
| C. | 能够电离出氢离子的化合物叫酸 | |
| D. | 胶体区别于其他分散系的本质特征是具有丁达尔效应 |
分析 A.电解质必须是化合物;
B.胶体分散质微粒直径在1nm-100nm间,形成的分散系为胶体;
C.水溶液中电离出的阳离子全部是氢离子的化合物为酸;
D.胶体区别于其他分散系最本质的特征是胶体是分散质粒子直径的大小.
解答 解:A.电解质必须是化合物,能在水溶液或熔融状态下导电的化合物是电解质,故A错误;
B.微粒直径在10-9 m-10-7m之间的分散质在分散剂中形成的分散系为胶体,故B正确;
C.能够电离出氢离子的化合物不一定叫酸,如NaHSO4溶液中电离出氢离子,属于盐,故C错误;
D.胶体区别于其他分散系最本质的特征是胶体是分散质粒子直径10-9-10-7m之间,丁达尔效应是特征性质,故D错误;
故选B.
点评 本题考查了电解质、胶体概念和性质分析判断,主要是胶体的特征性质和本质特征的掌握,题目难度不大.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4分子的比例模型: | B. | NH3的电子式: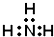 | ||
| C. | Ca2+的结构示意图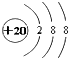 | D. | 次氯酸的结构式:H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸硫酸 H2SO3 | B. | 酸性氧化物干冰 CO | ||
| C. | 碱性氧化物氧化钙 CaO | D. | 盐苏打 NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ③④ | C. | ①② | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
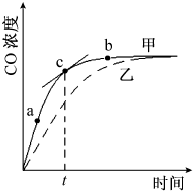 氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得.实验研究认为,该碳热还原反应分两步进行:①Al2O3在碳的还原作用下生成铝的气态低价氧化物X(X中Al与O的质量比为6.75:2);②在碳存在下,X与N2反应生成AlN.请回答:
氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得.实验研究认为,该碳热还原反应分两步进行:①Al2O3在碳的还原作用下生成铝的气态低价氧化物X(X中Al与O的质量比为6.75:2);②在碳存在下,X与N2反应生成AlN.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
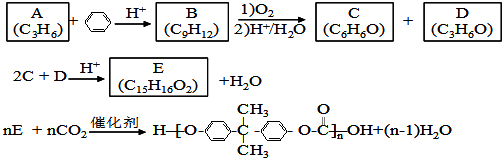
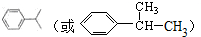 ;
;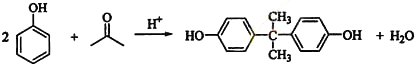 ;
;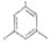 (写出结构简式).
(写出结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3<△H2<△H1<△H4<△H5 | B. | △H1<△H2<△H3<△H5<△H4 | ||
| C. | △H4<△H5<△H1<△H2<△H3 | D. | △H4<△H5<△H3<△H2<△H1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com