
模拟铁的电化学防护的实验装置如图所示,下列说法不正确的是

A.若X为碳棒,开关K置于A处可减缓铁的腐蚀
B.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀
C.若X为锌棒,开关K置于B处时,铁电极上发生的反应为2H++2e-=H2↑
D.若X为碳棒,开关K置于A处时,铁电极上发生的反应为2H++2e-=H2↑
科目:高中化学 来源:2017届山东省高三上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.向某溶液滴加K3[Fe(CN)6]溶液,若产生蓝色沉淀,说明溶液中有Fe2+
B.加入适量的NaOH 可除去NaHCO3溶液中混有的少量Na2CO3
C.某气体能使湿润的淀粉碘化钾试纸变蓝,则该气体一定是氯气
D.向某溶液滴加稀盐酸,生成的气体能使澄消石灰水变浑浊,则溶液中一定有CO32-或HCO3-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上第一次月考化学卷(解析版) 题型:选择题
设NA表示阿伏伽德罗常数,下列叙述中不正确的是
A.常温常压下,11.2LH2的物质的量小于0.5mol
B.2.4 g金属镁变成镁离子时失去的电子数为0.2NA
C.2 g氦气中含有的原子数为NA
D.标准状况下,18g水所含原子数为3NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:选择题
下列说法中,正确的是
A.强电解质的水溶液一定比弱电解质溶液的导电能力强
B.强电解质都是离子化合物,弱电解质都是共价化合物
C.强电解质的水溶液中不存在溶质分子
D.不溶性盐都是弱电解质,可溶性酸和具有极性键的化合物都是强电解质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:选择题
在一定温度下,下列叙述不是可逆反应A(g)+3B(g)  2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等;
②单位时间内amol A生成的同时生成3amol B;
③A、B、C的浓度不再变化;
④容积不变的密闭容器中混合气体的总压强不再变化;
⑤混合气体的物质的量不再变化;
⑥单位时间消耗amol A,同时生成3amol B;
⑦A、B、C的分子数目比为1:3:2。
A.②⑤ B.②⑦ C.①③ D.⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:选择题
图Ⅰ是NO2(g)+CO(g) CO2(g)+NO(g)反应过程中能量变化示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态.当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ,下列有关说法正确的是
CO2(g)+NO(g)反应过程中能量变化示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态.当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ,下列有关说法正确的是

A.一定条件下,向密闭容器中加入1molNO2(g)与1molCO(g)反应放出234 kJ热量
B.若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
C.若X表示反应时间,则Y表示的可能是混合气体的密度
D.若X表示温度则Y表示的可能是CO2物质的量浓度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学卷(解析版) 题型:实验题
右图为实验室某盐酸试剂瓶标签上的有关数据,是根据标签上的有关数据回答下列问题:
试根据标签上的有关数据回答下列问题:

⑴该浓盐酸中HCl的物质的量浓度为___________mol·L-1。
⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_________。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.40 mol/L的稀盐酸。
①容量瓶上需标有以下五项中的_________
A.温度 B.浓度 C.容量 D.压强 E.刻度线
②将下列操作填写完整,并排列其正确的操作顺序______________(字母表示,每个字母只能用一次);
A.用量筒准确量取浓盐酸___________ml,注入烧杯中,加入少量水(约30ml),用玻璃棒慢慢搅拌,使其混合均匀;
B.用30ml水洗涤烧杯2~3此,洗涤液均注入容量瓶,振荡;
C.将已冷却的盐酸沿玻璃棒注入___________中;
D.将容量瓶盖紧,颠倒摇匀;
E.改用_______加水,使溶液凹液面恰好与刻度线相切;
F.继续往容量瓶内小心加水,直到液面至刻度线下_________处。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上10月月考化学卷(解析版) 题型:填空题
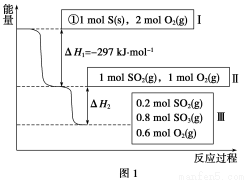
恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示
[已知:2SO2(g)+O2(g)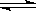 2SO3(g) ΔH=-196.6 kJ·mol-1]:
2SO3(g) ΔH=-196.6 kJ·mol-1]:
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:____________________。
(2)ΔH2=_____________________。
(3)恒温恒容时,1 mol SO2和2 mol O2充分反应,放出热量的数值比|ΔH2|________(填“大”、“小”或“相等”)。
(4)将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为__________,若溶液中发生了氧化还原反应,则该过程的离子方程式为______________________。
(5)向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2 和1 mol O2;(乙) 1 mol SO2 和0.5 mol O2;(丙) 2 mol SO3;恒温、恒容下反应达平衡时,下列关系一定正确的是( )
A.容器内压强p:p甲=p丙>2p乙
B.SO3的质量m:m甲=m丙>2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙>k乙
D.反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
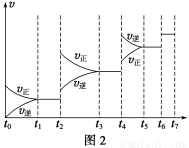
(6)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是__________;图中表示平衡混合物中SO3的含量最高的一段时间是____________。
(7)各阶段平衡时对应的平衡常数如下表所示:
t1~t2 | t3~t4 | t5~t6 | t6~t7 |
K1 | K2 | K3 | K4 |
K1、K2、K3、K4之间的关系为__________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上月考一化学试卷(解析版) 题型:填空题
(1)反应A(g)+B(g) 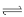 C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。

①该反应是___________反应(填“吸热”、“放热”)。
②当反应达到 平衡时,升高温度,A的转化率___________(填“增大”、“减小”或“不变”),原因是___________________
平衡时,升高温度,A的转化率___________(填“增大”、“减小”或“不变”),原因是___________________
(2)(6分)把3molA和2.5molB 混合,充入2L密闭容器中,发生下列反应:3A(g)+B(g)=xC(g
混合,充入2L密闭容器中,发生下列反应:3A(g)+B(g)=xC(g )+2D(g),经5秒钟反应
)+2D(g),经5秒钟反应 达到平衡,生成1 molD,并测得C的平均反应速率为0.1mol·L-1·s-1,则此反应中B的转化率为 ,C的化学计量数x为 ,A的平衡浓度为 。
达到平衡,生成1 molD,并测得C的平均反应速率为0.1mol·L-1·s-1,则此反应中B的转化率为 ,C的化学计量数x为 ,A的平衡浓度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com