

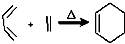 RCH2CH=CH2$→_{hv}^{Br_{2}}$RCHBrCH=CH2.请按要求回答下列问题:
RCH2CH=CH2$→_{hv}^{Br_{2}}$RCHBrCH=CH2.请按要求回答下列问题: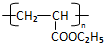 .
. .
. 均2个,反应④的化学方程式为
均2个,反应④的化学方程式为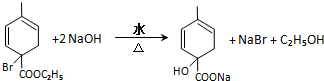 .
. .
. 分析 化合物A(C5H8)是形成天然橡胶的单体,则A为: ,由A与B的产物结构、结合反应信息可知,A与B发生加成反应,可知B为:CH2=CHCOOC2H5,反应①烯烃与溴发生加成反应生成
,由A与B的产物结构、结合反应信息可知,A与B发生加成反应,可知B为:CH2=CHCOOC2H5,反应①烯烃与溴发生加成反应生成 ,反应②为氢氧化钠醇溶液、加热条件下发生消去反应,反应③在光照条件下与溴发生取代反应,由信息可知,与碳碳双键相连的碳原子上的H原子被取代,C再氢氧化钠水溶液、加热条件下发生卤代烃的水解、酯的水解,再酸化得到C8H10O3,故C为一溴代物,由于分子中含-CH2,
,反应②为氢氧化钠醇溶液、加热条件下发生消去反应,反应③在光照条件下与溴发生取代反应,由信息可知,与碳碳双键相连的碳原子上的H原子被取代,C再氢氧化钠水溶液、加热条件下发生卤代烃的水解、酯的水解,再酸化得到C8H10O3,故C为一溴代物,由于分子中含-CH2,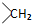 均2个,则C为:
均2个,则C为: ,C8H10O3为:
,C8H10O3为: ,据此进行解答.
,据此进行解答.
解答 解:化合物A(C5H8)是形成天然橡胶的单体,则A为: ,由A与B的产物结构、结合反应信息可知,A与B发生加成反应,可知B为:CH2=CHCOOC2H5,反应①烯烃与溴发生加成反应生成
,由A与B的产物结构、结合反应信息可知,A与B发生加成反应,可知B为:CH2=CHCOOC2H5,反应①烯烃与溴发生加成反应生成 ,反应②为氢氧化钠醇溶液、加热条件下发生消去反应,反应③在光照条件下与溴发生取代反应,由信息可知,与碳碳双键相连的碳原子上的H原子被取代,C再氢氧化钠水溶液、加热条件下发生卤代烃的水解、酯的水解,再酸化得到C8H10O3,故C为一溴代物,由于分子中含-CH2,
,反应②为氢氧化钠醇溶液、加热条件下发生消去反应,反应③在光照条件下与溴发生取代反应,由信息可知,与碳碳双键相连的碳原子上的H原子被取代,C再氢氧化钠水溶液、加热条件下发生卤代烃的水解、酯的水解,再酸化得到C8H10O3,故C为一溴代物,由于分子中含-CH2,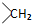 均2个,则C为:
均2个,则C为: ,C8H10O3为:
,C8H10O3为: ,
,
(1)反应①发生烯烃与溴的加成反应,反应③在光照条件下与溴发生取代反应,
故答案为:加成反应;取代反应;
(2)B为CH2=CHCOOC2H5,则B的分子式为C5H8O2,B含有碳碳双键,发生加聚反应生成高聚物,该高聚物的结构简式为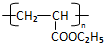 ,
,
故答案为:C5H8O2;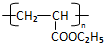 ;
;
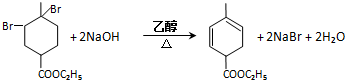
(3)反应②的化学方程式为: ,
,
故答案为: ;
;
(4)反应④的化学方程式为: ,
,
故答案为: ;
;
(5)A为 ,名称为:2-甲基-1,3-丁二烯,A的同分异构体满足:①环状,②核磁共振氢谱显示有2种氢原子,不可能为五元环、四元环,只能为三元环、含有一个碳碳双键,符合条件的同分异构体有:
,名称为:2-甲基-1,3-丁二烯,A的同分异构体满足:①环状,②核磁共振氢谱显示有2种氢原子,不可能为五元环、四元环,只能为三元环、含有一个碳碳双键,符合条件的同分异构体有: ,
,
故答案为:2-甲基-1,3-丁二烯; .
.
点评 本题考查有机物推断,题目难度较大,充分利用有机物的结构、分子式采取正、逆推法相结合进行推断,需要学生对给予的信息进行利用,熟练掌握官能团的性质与转化.


科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 选项 | X | Y |
| A | Na2CO3 | NaHCO3 |
| B | Al(OH)3 | Al2O3 |
| C | FeCl3 | FeCl2 |
| D | CuSO4 | Cu(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
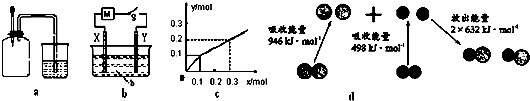
| A. | 如图a所示,集气瓶内充满Cl2和CH4的混合气体或NO2和O2的混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,并可能充满集气瓶 | |
| B. | Pt为电极,电解含0.10 mol M+和0.1 mol N3+(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图c,离子氧化能力M+>N3+>H+ | |
| C. | 如图b所示,X为铁棒,Y为铜棒,M为直流电源,当S闭合后,当b为NaOH溶液,X极附近产生白色沉淀时,电子从X极流入M | |
| D. | 图d为N2(g)和O2(g)生成NO(g)过程中的能量变化,则N≡N的键能为946kJ/mol,其热化学方程式为 N2(g)+O2(g)═2NO(g)△H=-180 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
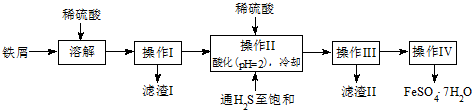
| 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 | |
| pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
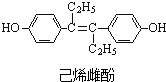
| A. | 与NaOH反应可生成化学式为C18H18O2Na2的化合物 | |
| B. | 聚己烯雌酚含有顺式和反式两种结构 | |
| C. | 1mol己烯雌酚最多可与7molH2发生加成反应 | |
| D. | 形成高分子 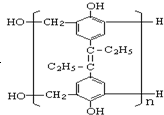 的单体中有己烯雌酚 的单体中有己烯雌酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| B. | 0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(H+)+c(Cl-)>c(NH4+)+c(OH-) | |
| D. | 0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com