
【化学—选修2:化学与技术】(15 分)氯碱工业是最基本的化学工业之一,离子膜电解法为目前普遍使用的生产方法,其生产流程如下图1 所示:
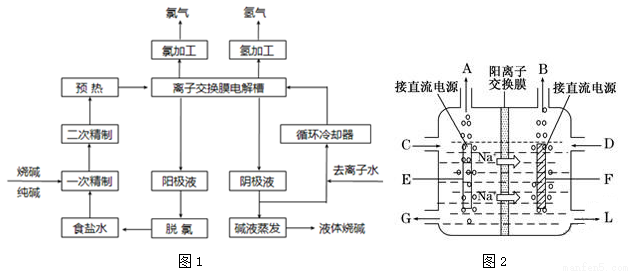
(1)该流程中可以循环的物质是 。
(2)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42-等无机杂质,所以在进入电解槽前需要进行两次精制, 写出一次精制中发生的离子方程式 、 ,若食盐水不经过二次精制,仍会有少量的Ca2+、Mg2+直接进入离子膜电解槽,这样产生什么后果是 。
(3)图2 是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极由碳钢网制成)。则B 处产生的气体是 ,E电极的名称是 极。电解总反应的化学方程式为 。
(4)从阳极槽出来的淡盐水中,往往含有少量的溶解氯,需要加入8%~9%的亚硫酸钠溶液将其彻底除去,该反应的离子方程式为 。
(5)已知在电解槽中,每小时通过1 安培的直流电理论上可以产生1.492 g 的烧碱,某工厂用300 个电解槽串联生产8 小时,制得30%的烧碱溶液(密度为1.342 吨/m3)113 m3,电解槽的电流强度1.45×104 A,该电解槽的电解效率为______ 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届山东省枣庄市高三9月阶段性学情检测化学试卷(解析版) 题型:选择题
现有十种物质:①水;②石墨;③氯气;④硫酸钡晶体;⑤醋酸;⑥二氧化碳;⑦氨水;⑧ 氯化钠固体;⑨熔化的氯化钠;⑩氯化钠溶液。请用序号按要求填空:
(1)其中能导电的是________
(2)属于强电解质的是______ 属于弱电解质的是________
(3)属于非电解质的是______
(4)既不是电解质也不是非电解质的是__________ 。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
物质中杂质(括号内为杂质)的检验、除杂的试剂或方法都正确的是
物质及其杂质 | 检验 | 除杂 | |
A | Cl2(HCl) | 湿润的淀粉KI试纸 | 饱和食盐水 |
B | NO(NO2) | 观察颜色或湿润的淀粉KI试纸 | 水 |
C | CO2(HCl) | AgNO3溶液(含稀硝酸) | 饱和Na2CO3溶液 |
D | NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 | 过量CO2 |
查看答案和解析>>
科目:高中化学 来源:2016届江汉油田海南海政学校高三月考化学试卷(解析版) 题型:选择题
在溶液中加入足量的Na2O2后仍能大量共存的离子组是
A.Na+、Fe2+、Cl-、SO42- B.K+、AlO2-、Cl-、SO42-
C.Ca2+、Mg2+、NO3-、HCO3- D.Na+、Cl-、CO32-、SO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高一下学期期末考试化学试卷(解析版) 题型:填空题
(6分)已知乳酸的结构简式为 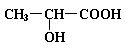 。试回答:
。试回答:
①乳酸分子中含有________和_________两种官能团(写名称);
②乳酸与足量金属钠反应的化学方程式为___________________;
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三7月月考化学试卷(解析版) 题型:选择题
下列叙述正确有几个
①晶体中不一定存在分子间作用力,但一定存在化学键
②液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
③向Fe(NO3)2溶液中通入过量的HI,最终Fe2+被氧化生成Fe3+
④将SO2通入紫色石蕊溶液,溶液先变红,后褪色
⑤将过量的二氧化碳气体通入硅酸钠溶液中,然后加热蒸干,再在高温下充分灼烧,最后得到的固体为碳酸钠和二氧化硅
A.0个 B.1个 C.2个 D.3个
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三上学期第一次质检化学试卷(解析版) 题型:选择题
下列各组离子能在指定溶液中大量共存的是
①无色溶液中:Al3+、Cl-、Na+、HCO3-、SO42-
②pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
③加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
④使pH试纸呈红色的溶液中:Fe3+、MnO4-、Na+、SO42-
⑤酸性溶液中:Fe2+、Al3+、NO3-、I-
A.①②④ B.①⑤ C.②③④ D.①②③
查看答案和解析>>
科目:高中化学 来源:2016届河南省郑州市新高三年级调研检测化学试卷(解析版) 题型:选择题
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是
A.Z与Y形成的化合物可作为耐高温材料
B.WY2能与碱反应,但不能与任何酸反应
C.原子半径按X、Y、Z、R、W的顺序依次增大
D.熔沸点:X2R>X2Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com