
(6分)铁及其化合物之间的相互转化可用下式表示: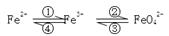
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液实现上述①的转化,要求产物纯净。可选用的试剂是 (选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+===Cu2++5Fe2++2S(CuFeS2中S为-2价)。
则下列说法正确的是 (选填序号);
a.从物质的组成来看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2既作氧化剂又作还原剂
d.当转移1 mol e- 时,有46 g CuFeS2参加反应
(3)高铁酸钾是一种新型、高效的绿色净水剂,其净水原理是 。
(6分)
(1)d(2分) (2)d(2分)
(3)高铁酸钾具有强氧化性,可以杀菌、消毒(1分),同时生成的Fe3+离子转化为Fe(OH)3胶体,能加速悬浮物沉降,起净化作用(1分)。
解析试题分析:(1)要使产物纯净,必须物质间发生反应后,没有杂质生成。A项有氯离子杂质生成,错误;b项铁与稀硫酸反应生成二价铁离子,不能把二价铁离子转化为三价铁离子,错误;c项硝酸能氧化二价铁离子生成三价铁离子,但溶液中还有杂质硝酸根离子,错误;d项双氧水能氧化二价铁离子生成三价铁离子,同时有水生成,水是原溶液的成分,所以不是杂质,正确。故选d。
(2)a项合金是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质,所以黄铜矿不是合金,错误;b项CuFeS2中铁元素的化合价为+2价,生成物中Fe2+的化合价为+2价,所以不是所有铁元素均被还原,错误;c项CuFeS2中只有S元素的化合价只有降低,其他元素的化合价不变,所以CuFeS2只作还原剂,错误;d项根据反应CuFeS2+4Fe3+=Cu2++5Fe2++2S,在这个反应中转移4mol电子,生成184g CuFeS2。则转移1 mol e- 时,有 46g CuFeS2参加反应。故d正确。
(3)高铁酸钾( K2FeO4)中Fe的化合价是+6价,具有强氧化性,能杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体,能吸附水中杂质,所以高铁酸钾作为水处理剂发挥的作用是净水、消毒。
考点:铁盐和亚铁盐的相互转变;氧化还原反应。
点评:本题考查了铁盐和亚铁盐的相互转化,难度不大,注意二价铁离子和三价铁离子的检验是高考的热点,三价铁离子能使KSCN变红色。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
| ① |
| ④ |
| ② |
| ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 铁及其化合物之间的相互转化可用下式表示:①②③④
铁及其化合物之间的相互转化可用下式表示:①②③④| ① |
| ④ |
| ② |
| ③ |
2- 4 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省潍坊市高三3月模拟考试(一模)化学试卷(解析版) 题型:简答题
铁及其化合物之间的相互转化可用下式表示:
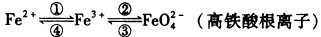
回答下列有关问题:
(1)铁元素位于元素周期表的第四周期第Ⅷ族,原子序数是26,最外层有2个电子。元素铁的原子结构示意图是??????????? 。
(2)检验硫酸铁溶液中是否存在Fe2+的方法是
(3)
(4)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为Fe3+。Na2FeO4之所以能净水,除了能消毒杀菌外,另一个原因是(结合离子方程式说明) ??????????????????? 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年重庆市高三上学期期中考试理综化学试卷(解析版) 题型:填空题
铁及其化合物之间的相互转化可用下式表示:

回答下列有关问题:
(1)铁元素在周期表中的位置是___________________________。
(2)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净,可选用的试剂是________(选填序号)。
A.Cl2 B.Fe C.HNO3 D.H2O2
(3)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应CuFeS2+4Fe3+=Cu2++5Fe2++2S(CuFeS2中S为-2价),下列说法正确的是________(选填序号)。
A.从物质分类的角度看,黄铜矿属于合金
B.反应中,所有铁元素均被还原
C.反应中,CuFeS2 既作氧化剂又作还原剂
D.当转移1 mol电子时,46 g CuFeS2参加反应
(4)下述反应中,若FeSO4和O2的系数比为2︰1,试配平下列方程式:
FeSO4 + K2O2 → K2FeO4 + K2O + K2SO4 + O2↑
(5)向某稀HNO3和Fe(NO3)3的混合溶液中逐渐加入铁粉,产生无色气体, 该气体遇空气变红棕色,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如右图所示。则混合溶液中HNO3和Fe(NO3)3的物质的量浓度之比为__________。

(6)某同学将铁与水蒸气高温反应后的固体物质溶解在过量盐酸中,如何判断所得溶液中是否含有Fe3+ ? ___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2010年福建省高二第二学期期末考试化学试题 题型:填空题
(附加题)(8分)铁及其化合物之间的相互转化可用下式表示:
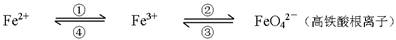
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净。可选用的试剂是 (选填序号);
A.Cl2 B.Fe C.HNO3 D.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2 + 4Fe3+ = Cu2+ + 5Fe2+ + 2S。(CuFeS2中S为—2价)
则下列说法正确的是 (选填序号);
A.从物质分类的角度看,黄铜矿属于合金
B.反应中,所有铁元素均被还原
C.反应中,CuFeS2 既作氧化剂又作还原剂
D.当转移1mol电子时,46 g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2 :1,试配平下列方程式:
FeSO4 + K2O2 → K2FeO4 + K2O + K2SO4 + O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3胶体。高铁酸钾作为水处理剂发挥的作用是_______、_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com