
| A. | 化学反应除了生成新的物质外,只伴随着热量的变化 | |
| B. | 物质燃烧不一定是放热反应,放热的化学反应不需要加热就能发生 | |
| C. | 太阳能、氢能、生物质能属于新能源 | |
| D. | 化石燃料是一次能源,乙醇是不可再生能源 |
分析 A、化学反应在发生物质变化的同时还伴随着能量的变化;
B、反应放热和吸热只决定与反应物和生成物的能量高低,与反应条件无关;
C、太阳能、潮汐能、风能、氢能、生物质能等都是可再生、无污染的新能源;
D、使用完后不可能在短时间内形成,是不可再生能源.
解答 解:A、化学反应在发生物质变化的同时还伴随着能量的变化,其中能量包括热量、光能等能量,故A错误;
B、燃烧都是放热反应,但必须加热到物质的着火点,故B错误;
C、太阳能、氢能、生物质能都属于新能源,故C正确;
D、化石能源使用完后不可能在短时间内形成,是不可再生能源,属于一次能源,乙醇是可再生能源,故D错误.
故选C.
点评 本题考查常见的能量转换形式,以及化学反应中能量变化的原因,可以根据教材知识来回答,较简单.


科目:高中化学 来源: 题型:填空题
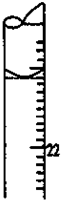 某学生用0.1000mol•L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
某学生用0.1000mol•L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 春节燃放爆竹对环境无污染 | |
| B. | “酸雨”是由大气中的碳、氮、硫的氧化物溶于雨水造成 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | 光化学烟雾的产生与人为排放大气污染物氮氧化物无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③④ | B. | 只有②③⑦ | C. | 只有①③⑥ | D. | 只有⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
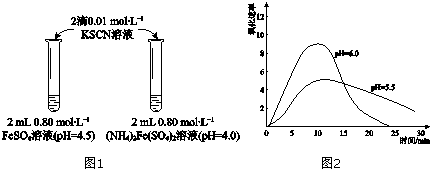
| 物质 | 0min | 1min | 1h | 5h |
| FeSO4 | 淡黄色 | 桔红色 | 红色 | 深红色 |
| (NH4)2Fe(SO4)2 | 几乎无色 | 淡黄色 | 黄色 | 桔红色 |
| 操作 | 现象 |
| 取取2mLpH=4.0的0.80mol•L-1FeSO4溶液,加加2滴0.01mol•L-1KSCN溶液,观察. | 与实验Ⅰ中(NH4)2Fe(SO4)2溶液现象相同. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)根据无机含氧酸的酸性规律,将下列四种无机含氧酸按酸性相近两两组成一组,它们是①和④;②和③.(用序号表示)
(1)根据无机含氧酸的酸性规律,将下列四种无机含氧酸按酸性相近两两组成一组,它们是①和④;②和③.(用序号表示)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ③④⑤ | C. | ③⑤⑥ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
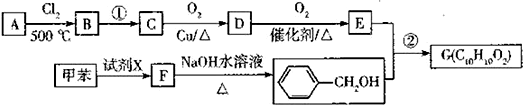
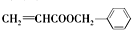 .
.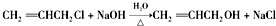 .
.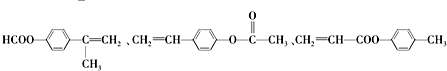 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com