
 如图为元素周期表的一部分,A、B、C均为短周期元素.B的最高价氧化物的水化物为H3BO4,则A、B、C依次是( )
如图为元素周期表的一部分,A、B、C均为短周期元素.B的最高价氧化物的水化物为H3BO4,则A、B、C依次是( )| A. | C、A1、P | B. | N、Si、S | C. | C、P、O | D. | F、S、Ar |
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
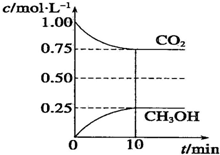 在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ.mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ.mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(NH3):n (O2)=4:5 | |
| B. | 反应达到平衡后,对体系一直进行加压,平衡总是向逆向移动 | |
| C. | 反应达到平衡时,若向压强固定的密闭容器中充入稀有气体,平衡不移动 | |
| D. | 当v正(NH3):v正(NO)=1:1 时,说明该化学反应已经达到平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 含苯酚的工业废水的处理流程如图所示.
含苯酚的工业废水的处理流程如图所示. ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池工作时,电子由Al电极经外电路流向Li电极 | |
| B. | 该电池的电池反应式为:2Li+FeS═Li2S+Fe | |
| C. | 负极的电极反应式为Al-3e-═Al3+ | |
| D. | 电解质溶液可以是氢氧化钠溶液或者稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题










查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 步骤(1)产物中残留的苯酚可用FeCl3溶液检验 | |
| B. | 反应(1)和(2)均为取代反应 | |
| C. | 苯酚、苯氧乙酸和菠萝酯均可与NaOH溶液发生反应,均有酸性 | |
| D. | 与苯氧乙酸互为同分异构体,能使FeCl3溶液显紫色,并能发生水解反应但不发生银镜反应的芬香族化合物共有6种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com