
有关物质的转化关系如图所示(部分物质和条件已略去).A是海水中含量最多的盐,B、E、F是气体单质,C是金属单质,X是能使湿润红色石蕊试纸变蓝的气体,Y是最常见的无色液体.

请回答下列问题:
(1)X的化学式为 NH3 .
(2)E的电子式为  .
.
(3)写出C与Y反应的化学方程式: 2Na+2H2O=2NaOH+H2↑ .
(4)写出D溶液与G溶液反应的离子方程式: NH4++OH﹣ NH3↑+H2O .
NH3↑+H2O .
| 无机物的推断.. | |
| 专题: | 推断题. |
| 分析: | 海水中含量最多的是氯化钠,A是海水中含量最多的盐,则A为NaCl,C是金属单质,电解NaCl得到金属C,则C为金属Na,B为氯气;Y是最常见的无色液体、F是气体单质,钠能够与液态反应生成的气体为氢气,Y为水、G为NaOH;X是能使湿润红色石蕊试纸变蓝的气体,则X一定为碱性气体氨气,E为气体单质,E与Y氢气反应生成氨气,则E为氮气;D+G(NaOH) |
| 解答: | 解:A是海水中含量最多的盐,则A为NaCl,C为金属单质,电解NaCl得到金属C,发生反应为:2NaCl(熔融) (1)X是能使湿润红色石蕊试纸变蓝的气体,X为碱性气体,所以X只能为氨气,化学式为NH3, 故答案为:NH3; (2)根据以上分析可知,E为气体单质N2,氮气分子中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气的电子式为: 故答案为: (3)根据分析可知,C为Na、Y为H2O,则钠与水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑, 故答案为:2Na+2H2O=2NaOH+H2↑; (4)D为NH4Cl,G为NaOH,氢氧化钠与氯化铵溶液加热生成氨气和氯化钠,反应的离子方程式为:NH4++OH﹣ 故答案为:NH4++OH﹣ |
| 点评: | 本题考查无机物推断,涉及常见元素单质及其化合物性质,“X是能使湿润红色石蕊试纸变蓝的气体、A是海水中含量最多的盐”等是推断突破口,再结合转化关系推断,需要学生熟练掌握元素化合物知识,题目难度中等. |


科目:高中化学 来源: 题型:
在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内的分压与反应温度的关系如下图所示(已知气体的分压之比等于物质的量之比)。
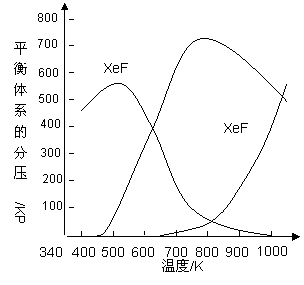
(1)420K时,发生反应的化学方程式为:____________________________;若反应中消耗l mol Xe,则转移电子______mol。
(2)600~800K时,会发生反应:
XeF6(g) XeF4(g)+ F2(g),
XeF4(g)+ F2(g),
该正反应为______反应(填“放热”或“吸热”)。理由是______________________________。
(3)900K时,容器中存在的组分有________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机化合物A的结构简式如下:
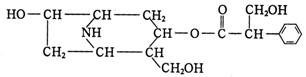
请回答下列问题:
(1)A的分子式是 。
(2)A在NaOH溶液中加热反应得到B和C,C分子中含有苯环。B的结构简式是 。
(3)室温下,C用稀盐酸酸化得到E,E的结构简式是 。
(4)在下列物质中,能与E发生化学反应的是(填写序号) 。
①溴水 ②FeCl3溶液 ③Na2CO3溶液 ④丁烷
(5)写出在铜作催化剂时,E与氧气反应的化学方程式:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁的快速发展方便了人们的出行.工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:2Al+Fe2O3 2Fe+Al2O3,其中Al是( )
2Fe+Al2O3,其中Al是( )
|
| A. | 氧化剂 | B. | 还原剂 |
|
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
N2+3H2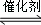 2NH3,是工业上制造氮肥的重要反应.下列关于该反应的说法正确的是( )
2NH3,是工业上制造氮肥的重要反应.下列关于该反应的说法正确的是( )
|
| A. | 增加N2的浓度能加快反应速率 |
|
| B. | 降低体系温度能加快反应速率 |
|
| C. | 使用催化剂不影响反应速率 |
|
| D. | 若反应在密闭容器中进行,N2和H2能100%转化为NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.金属氧化物一定是碱性氧化物 B.非金属氧化物一定是酸性氧化物
C.只有在标准状况下,气体的摩尔体积才能为22.4L/mol
D.非电解质在水溶液中和熔融状态下均以分子形式存在,因而不能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
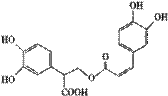 迭香酸有很强的抗氧化性,对癌症和动脉硬化的预防起到一定作用,其结构如右图所示。下列叙述正确的是
迭香酸有很强的抗氧化性,对癌症和动脉硬化的预防起到一定作用,其结构如右图所示。下列叙述正确的是
A.迷迭香酸的分子式为C18H15O8
B.迷迭香酸可以发生加成、取代、消去、显色反应
C.1mol迷迭香酸跟H2反应,最多消耗8mol H2
D.1mol迷迭香酸与足量NaOH溶液反应,最多消耗6mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com