
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:问答题
| 催化剂 |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CaCO3?Ca2++CO32- | B.H2CO3?2H++CO32- |
| C.NH3?H2O?NH3+H2O | D.H2SO3?H++HSO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.次氯酸的电离方程式:HClO?H++ClO- |
| B.只有熵增加的过程才能自发进行 |
| C.HS-水解离子方程式:HS-+H2O?H3O++S2- |
| D.已知中和热为57.3kJ?mol-1,稀硫酸与氢氧化钠稀溶液反应的热化学方程式:H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(l)△H=-114.6kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaHCO3=Na++HCO3- | B.NaHSO4═Na++H++SO42- |
| C.H2SO4═2H++SO42- | D.KClO3═K++Cl-+3O2- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
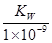 mol/L
mol/L查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1 mol·L-1CH3COONa溶液中:c(CH3COO-)+c(CH3COOH)=0.1 mol·L-1 |
| B.浓度均为0.1 mol·L-1 Na2CO3溶液和稀盐酸等体积混合后的溶液中: c(CO 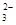 )+c(OH-)=c(H+)+c(H2CO3) )+c(OH-)=c(H+)+c(H2CO3) |
| C.25 ℃时,pH=9.4、浓度均为0.1 mol·L-1的HCN与NaCN的混合溶液中: c(Na+>c(CN-)>c(HCN)>c(OH-) |
| D. 3.0 L 0.1 mol·L-1 NaOH溶液中缓慢通入CO2至溶液增重8.8 g时,溶液中: |
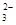 )>c(HCO
)>c(HCO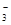 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com