
甲乙丙是三种不含相同离子的可溶性电解质。他们所含的离子如表所示。取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)<c(乙)<c(丙),下列说法正确的是
阳离子 | Na+ NH4+ Fe3+ |
阴离子 | OH- Cl- SO42- |
A、甲中一定含有Na+ B、乙中一定含有NH4+
C、丙中一定含有 Fe3+ D、丙中一定含有SO42-
科目:高中化学 来源:2016届甘肃省天水市高三上学期第三次测试化学试卷(解析版) 题型:选择题
下列各组离子在指定溶液中,一定能大量共存的是
A.加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,SO42-
B.含有NaClO的溶液中:K+, Al3+,Br-,S2-
C.澄清透明溶液:Cu2+,SO42-,HCO3-,H+
D.使甲基橙变红的溶液中:Fe2+,MnO4-,Na+,SO42-
查看答案和解析>>
科目:高中化学 来源:2016届江西省高安市高三上学期第二次段考化学试卷(解析版) 题型:实验题
高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下:MnO2熔融氧化:3MnO2+ KClO3+ 6KOH  3K2MnO4+ KCl+3H2O;
3K2MnO4+ KCl+3H2O;
K2MnO4歧化:3K2MnO4+ 2CO2=2KMnO4+ MnO2↓+2K2CO3。
已知K2MnO4溶液显绿色。请回答下列问题:
(1)MnO2熔融氧化应放在 中加热(填仪器编号)。
①烧杯 ②瓷坩埚 ③蒸发皿 ④铁坩埚
(2)在MnO2熔融氧化所得产物的热浸取液中通入CO2气体,使K2MnO4歧化的过程在如图装置中进行,A、B、C、D、E为旋塞,F、G为气囊,H为带套管的玻璃棒。
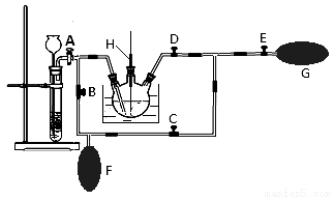
①为了能充分利用CO2,装置中使用了两个气囊。当试管内依次加入块状碳酸钙和盐酸后,关闭旋塞B、E,微开旋塞A,打开旋塞C、D,往热K2MnO4溶液中通入CO2气体,未反应的CO2被收集到气囊F中。待气囊F收集到较多气体时,关闭旋塞 ,打开旋塞 ,轻轻挤压气囊F,使CO2气体缓缓地压入K2MnO4溶液中再次反应,未反应的CO2气体又被收集在气囊G中。然后将气囊G中的气体挤压入气囊F中,如此反复,直至K2MnO4完全反应。
②检验K2MnO4歧化完全的实验操作是 。
(3)利用氧化还原滴定法进行高锰酸钾纯度分析,原理为:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
现称取制得的高锰酸钾产品7.245g,配成500mL溶液,用移液管量取25.00 mL待测液,用0.1000 mol·L-1草酸钠标准溶液液进行滴定,终点时消耗标准液体积为50.00mL(不考虑杂质的反应),则高锰酸钾产品的纯度为 (保留4位有效数字,已知M(KMnO4)=158g·mol-1)。若移液管用蒸馏水洗净后没有用待测液润洗或烘干,则测定结果将 。(填“偏大”、“偏小”、“不变”)
查看答案和解析>>
科目:高中化学 来源:2016届山东省临沂市高三上学期第一次月考化学试卷(解析版) 题型:选择题
2015年6月5日世界“环境日”中国的主题是“践行绿色生活”.下列不符合这一主题的是
A.从自身做起,从身边小事做起,减少超前消费、炫耀性消费、奢侈性消费和铺张浪费现象
B.减少温室气体的排放,倡导“绿色低碳”的生活
C.少开私家车,提倡“绿色出行”
D.向空气中喷洒烧碱溶液,避免酸雨的发生
查看答案和解析>>
科目:高中化学 来源:2016届陕西省西安市高三上学期10月月考化学试卷(解析版) 题型:选择题
为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气.下列关于Na2O2的叙述正确的是
A. Na2O2中阴、阳离子的个数比为1:1
B. Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
C. Na2O2分别与水及CO2反应产生相同量的O2时,转移电子的物质的量相等
D. Na2O2的漂白原理与SO2的漂白原理相同
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市高三上学期10月月考化学试卷(解析版) 题型:选择题
在容积相同的甲、乙两个密闭容器中,均分别充入2molSO2和1molO2,发生反应:2SO2+O2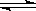 2SO3,在相同温度下,若甲容器始终保持体积不变,乙容器始终保持压强不变,达平衡时测得甲容器中SO2的转化率为25%,则乙容器中SO2的转化率
2SO3,在相同温度下,若甲容器始终保持体积不变,乙容器始终保持压强不变,达平衡时测得甲容器中SO2的转化率为25%,则乙容器中SO2的转化率
A.25% B.小于25% C.大于25% D.无法确定
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上期中测试化学试卷(解析版) 题型:填空题
(10分)常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:
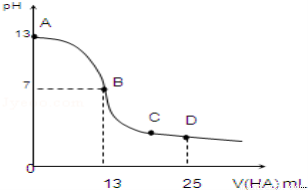
(1)写出MOH的电离方程式:__________________
(2)MOH与HA恰好完全反应时,溶液呈________性(填“酸”、“碱”或“中”),理由是(用离子方程式表示):__________;此时,混合溶液中由水电离出的c(H+)_________0.2mol/L HA溶液中由水电离出的c(H+)(填“>”“<”或“=”).
(3)写出B点,混合溶液中各离子浓度的大小关系B点____________.
(4)D点时,溶液中c(A﹣)+c(HA)__________2c(M+)(填“>”、“<”或“=”).
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三上学期期中测试理综化学试卷(解析版) 题型:选择题
在下列溶液中,各组离子一定能够大量共存的是
A.c(H+) = 10-12 mol/L的溶液:K+、Ba2+、Cl-、Br-
B.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
C.碳酸氢钠溶液:K+、SO42-、Cl-、H+
D.使酚酞试液变红的溶液: Na+、Cl-、SO42-、Fe3+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省清远市高二上学期10月月考化学试卷(解析版) 题型:选择题
一定温度下反应:A2(g)+3 B2(g)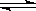 2 AB3(g) (每生成2 mol AB3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol A2和3 mol B2,达平衡时放出热量为Q1,②通入2 mol A2和6 mol B2,达平衡时放出热量为Q2,则下列关系正确的是
2 AB3(g) (每生成2 mol AB3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol A2和3 mol B2,达平衡时放出热量为Q1,②通入2 mol A2和6 mol B2,达平衡时放出热量为Q2,则下列关系正确的是
A.Q2 = 2 Q1 B.2Q1 < Q2
C.Q1 < Q2 < 92.4 kJ D.Q1 = Q2 < 92.4 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com