
科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 1将一小块金属钠放入滴有酚酞溶液的冷水中; 2将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液; 3将一小段镁带投入稀盐酸中; 4将一小片铝投入稀盐酸中. |
| 实验现象 | A剧烈反应,迅速生成大量的气体 B浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红 C反应不剧烈,产生无色气体 D有气体产生,溶液变成红色 |
| 实验步骤 | 1 | 2 | 3 | 4 |
| 实验现象 | B B |
D D |
A A |
C C |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013届河南省灵宝市第三高级中学高三上学期第三次质量检测化学试卷(带解析) 题型:实验题
(Ⅰ)(8分)某无色溶液中可能含有Na+、SO42— 、MnO4—、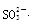 、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
①用pH试纸检验,溶液pH>7;
②向溶液中滴加氯水,无气体产生,再加入CCl4振荡、静置,CCl4层呈橙红色,用分液漏斗分液;
③向分液后的水溶液中加入AgNO3和HNO3混合液,有白色沉淀产生。
④另取原溶液少量加入Ba(NO3)2和盐酸的混合液,产生白色沉淀。
回答下列问题:
(1)溶液中肯定含有的离子是 ;肯定没有的离子是 。
⑵写出步骤②中的离子方程式 。
(Ⅱ)(6分)SO2气体通入滴有酚酞的NaOH溶液,红色逐渐褪去,可能的原因:
① ② 。
简述设计实验证明: 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省资阳市高三第二次高考模拟考试理综化学试卷(解析版) 题型:选择题
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,蓝色溶液变为棕色。再向反应后的溶液中通入过量的SO2气体,溶液变成无色。则下列说法正确的是
A.滴加KI溶液时,KI被氧化,CuI是氧化产物
B.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性
C.通入22.4 L SO2参加反应时,有2 NA个电子发生转移
D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省灵宝市高三上学期第三次质量检测化学试卷(解析版) 题型:实验题
(Ⅰ)(8分)某无色溶液中可能含有Na+、SO42—
、MnO4—、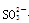 、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
①用pH试纸检验,溶液pH>7;
②向溶液中滴加氯水,无气体产生,再加入CCl4振荡、静置,CCl4层呈橙红色,用分液漏斗分液;
③向分液后的水溶液中加入AgNO3和HNO3混合液,有白色沉淀产生。
④另取原溶液少量加入Ba(NO3)2和盐酸的混合液,产生白色沉淀。
回答下列问题:
(1)溶液中肯定含有的离子是 ;肯定没有的离子是 。
⑵写出步骤②中的离子方程式 。
(Ⅱ)(6分)SO2气体通入滴有酚酞的NaOH溶液,红色逐渐褪去,可能的原因:
① ② 。
简述设计实验证明: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com