
| A、若根据反应“H2+Cl2=2HCl”设计成燃料电池,既可发电同时还可用于制备盐酸 |
| B、氯气溶于水达到平衡后,若其他条件不变,加入少量水,水的电离平衡向正向移动 |
| C、25℃时,任何稀溶液中由水电离出的c(H+)和c(OH-)的乘积都为1×10-14 mol2?L-2 |
| D、冰醋酸中逐滴加水,则溶液的导电性先增大后减小 |


科目:高中化学 来源: 题型:
| A、原子半径:x>y |
| B、电负性:x>y |
| C、离子半径:x<y |
| D、第一电离:x<y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分馏、裂化、裂解是利用化学变化来炼制加工石油的三种重要方法 |
| B、蛋白质、淀粉、纤维素都能在人体内水解并提供能量 |
C、使用聚乙烯塑料制品比使用聚乳酸 (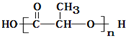 )塑料制品更环保 )塑料制品更环保 |
| D、酶催化反应具有高效、专一、条件温和等特点,化学模拟生物酶对环境保护、节能减排具有重要意义 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 沸腾炉炉度/℃ | 560 | 580 | 600 | 620 | 640 | 660 | |
| 生成物 | 水溶性Cu% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
| 酸溶性Cu% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 | |
| 酸溶性Fe% | 8.56 | 6.72 | 3.46 | 2.78 | 2.37 | 2.28 | |
| A、反应中有二氧化硫生成 |
| B、产物中铜元素主要以氧化物形式存在 |
| C、随温度升高,铁的氧化物在酸中的溶解度降低 |
| D、温度高于600~620℃生成物中水溶性Cu(%)下降的原因是水溶性铜分解所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2+3H2?2NH3△H<0;工业上采用20MPa至50MPa的高压条件 | ||||||||
B、
| ||||||||
C、 | ||||||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| B、FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
| C、三氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+ |
| D、AlCl3溶液中加入足量的NaOH溶液:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com