
向盛有一定量氢氧化钠溶液的烧杯中通入标准状况下448mL氮气和二氧化碳的混合气体后得到溶液A,在溶液A中逐滴加入0.1mol/L的稀盐酸至过量,并将溶液加热,产生的二氧化碳气体的物质的量与加入稀盐酸的体积的关系如图所示
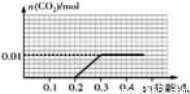
(忽略二氧化碳的溶解和氯化氢的挥发).下列说法正确的是
A.原混合气体中氮气与二氧化碳体积之比为1:4
B.在逐滴加入稀盐酸产生二氧化碳之前,发生的离子反应为CO32-+H+═HCO3-
C.溶液A中含有0.01molNaOH和0.01molNa2CO3
D.当加入0.1L稀盐酸时,此时溶液中离子浓度大小关系为
c(Na+)>c(Cl-)=c(CO32-)>c(OH-)>c(H+)
C
【解析】
试题分析:A.n(混合气体)=0.448L÷22.4L/mol=0.02mol.根据图像可知:n(CO2)=0.01mol,所以n(N2)=0.01mol。原混合气体中氮气与二氧化碳物质的量的比1:1.由于气体的体积比等于物质的量的比,故V(N2):v(CO2)=1:1.错误。B.产生气体的反应方程式为Na2CO3+ HCl=NaCl+ NaHCO3;NaHCO3+HCl=NaCl+H2O+ CO2↑。可见二者消耗的HCl物质的量相等。由于产生气体消耗的HCl体积是0.1L,所以发生第一个反应消耗的HCl也是0.1L。但根据图像可知在放出气体前消耗HCl的体积为0.2L,说明在溶液中还存在NaOH,因此,首先发生的反应是NaOH+HCl=NaCl+ H2O。故在逐滴加入稀盐酸产生二氧化碳之前,发生的离子反应为H++OH-=H2O ;CO32-+H+═HCO3-。错误。C.n(CO2)=n(Na2CO3)=0.01mol;n(NaOH)=n(HCl)=0.1L×0.1mol/L=0.01mol。故溶液A中含有0.01molNaOH和0.01molNa2CO3。正确。D.当加入0.1L稀盐酸时,发生反应:NaOH+HCl=NaCl+ H2O。因此该溶液为NaCl和Na2CO3按照1:1物质的量的比的混合溶液。根据物料守恒可知c(Na+)>c(Cl-)=c(CO32-)+ c(HCO3-)+ c(H2CO3)。c(CO32-)水解消耗水电离产生的H+,使溶液显碱性;而且在溶液中还存在水的电离,因此c(OH-)>c(H+).但是盐的水解程度是微弱的,所以c(CO32-)>c(OH-)。因此在该溶液中的离子浓度关系为c(Na+)>c(Cl-)>c(CO32-)c(OH-)>c(H+)。
考点:考查混合气体与碱反应得到的溶液的成分、离子浓度的大小比较、离子方程式的书写的知识。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源:2013-2014江苏省南京市高一下学期期末学情调研测试化学试卷(解析版) 题型:选择题
下列物质不属于高分子化合物的是
A.淀粉 B.纤维素 C.乙酸 D.聚乙烯
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏宿迁市高一下学期期末测试化学试卷(解析版) 题型:实验题
(12分)完成以下实验:①用右图所示的装置制取溴乙烷;②进行溴乙烷的性质实验。在试管I中依次加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水。加热试管I至微沸状态数分钟后,冷却。试回答下列问题:

(1)试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式 。
(2)试管I中反应除了生成溴乙烷,还可能生成的有机物有 _ 、
(写出两种有机物的结构简式)。
(3)溴乙烷的沸点较低,易挥发,为了使溴乙烷冷凝在试管Ⅱ中,减少挥发,上图中采取的措施有 、 _。
(4)在进行溴乙烷与NaOH乙醇溶液共热的性质实验时,把生成的气体通过下图所示的装置。用下图装置进行实验的目的是 _;下图中右边试管中的现象是 ;水的作用是 。

查看答案和解析>>
科目:高中化学 来源:2013-2014江苏宿迁市高一下学期期末测试化学试卷(解析版) 题型:选择题
将金属钠分别投入下列物质的稀水溶液中,能生成白色沉淀的是
A.HCl B.K2SO4 C.MgCl2 D.CuCl2
查看答案和解析>>
科目:高中化学 来源:2013-2014广西贵港市毕业班5月高考冲刺模拟理综化学试卷(解析版) 题型:实验题
(15分)实验室以废铜屑为原料制取碱式碳酸铜【Cu2(OH)2CO3】的步骤如下:
步骤一:废铜屑制硝酸铜
如图,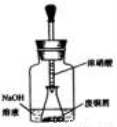
用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
步骤三:碱式碳酸铜的组成测定
碱式碳酸铜可表示为:xCuCO3 ·yCu (OH)2 ·zH2O,可采用氢气还原法来确定,其反应原理为:
xCuCO3 ·yCu (OH)2 ·zH2O + H2→ Cu + CO2 + H2O(未配平)
完成下列填空:
(1)步骤一中,反应开始时,瓶内的现象是 ,
用该装置制取硝酸铜,好处是 。
(2)步骤二中,水浴加热所需仪器有 、 (加热、夹持仪器、石棉网除外);洗涤的目的是 。
(3) 步骤三中,①以字x、y、z母为系数,配平氢气还原法的化学方程式:
xCuCO3 ·yCu (OH)2 ·zH2O+ H2→ Cu+ CO2+ H2O
②称取24.0g某碱式碳酸铜样品,充分反应后得到12.8 g残留物,生成4.4g二氧化碳和7.2g水。该样品中结晶水质量为 g,化学式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014广西贵港市毕业班5月高考冲刺模拟理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.所谓低碳经济,是指在可持续发展理念指导下,尽可能地减少光化学污染气体的排放
B.汽油、柴油和植物油都是碳氢化合物
C.只由一种元素组成的物质,一定是纯净物
D.化学反应的实质就是旧化学键的断裂、新化学键形成过程
查看答案和解析>>
科目:高中化学 来源:2013-2014广西桂林市下学期高二年级期末考试化学试卷(解析版) 题型:填空题
(8分)按要求填写空白:
(1)写出醋酸钠在水中发生水解反应的离子方程式:____________。
(2)浓度均为0.1mol/L的下列4种物质的水溶液:
①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵
pH由大到小的顺序是_________(填数字序号)。
(3)在①H2O ②HCHO ③Cl2 ④C2H2 ⑤CCl4分子中:
全部以非极性键结合的非极性分子是_________(填数字序号,下同);
全部以极性键相结合,具有V形分子立体构型的是________;
中心原子为sp3杂化的非极性分子是_________;
中心原子为sp2杂化的极性分子是________;
既有极性键又有非极性键的非极性分子是_____________。
查看答案和解析>>
科目:高中化学 来源:2013-2014广西桂林市下学期高二年级期末考试化学试卷(解析版) 题型:选择题
符合下列情况的化学反应一定能自发进行的是
A. △H<0、△S>0 B. △H<0、△S<0
C. △H>0、△S<0 D. △H>0、△S>0
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
分类是化学学习与研究的常用方法,下列分类正确的是 ( )
| A.Na2O、CaO、Al2O3均属于碱性氧化物 |
| B.根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质 |
| C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D.烧碱、纯碱均属于碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com