
化学与生产、生活密切相关,下列对有关现象及事实的解释正确的是( )
现象或事实 | 主要原因 | |
A | 燃煤中添加适量CaO可减少SO2排放量 | 燃烧中硫元素转化为CaSO3 |
B | 聚氯乙烯薄膜不能用于包装食品 | 会造成白色污染 |
C | 夏天雷雨过后感觉到空气特别的清新 | 空气中O3含量增加、尘埃减少 |
D | 蒸熟的糯米在适当条件可转化为香甜可口的甜酒 | 部分淀粉水解生成葡萄糖与乙醇 |
科目:高中化学 来源:2015-2016学年黑龙江双鸭山一中高二下期中化学试卷(解析版) 题型:实验题
液晶高分子材料应用广泛.新型液晶基元﹣化合物Ⅳ的合成线路如下:
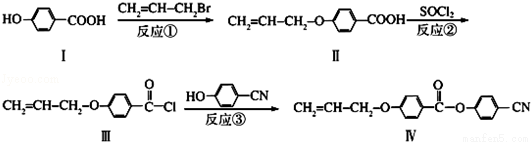
(1)化合物Ⅰ的分子式为 ,含有的官能团 ,1mol化合物Ⅰ完全燃烧消耗标准状况下 O2 L。
(2)CH2=CH﹣CH2Br与NaOH水溶液反应的化学方程式为 (注明条件)。
(3)下列关于化合物Ⅱ的说法正确的是 (填字母)。
A.能与FeCl3溶液反应呈紫色 B.属于烯烃
C.最多能与4mol H2发生加成反应 D.一定条件下能发生加聚反应
(4)反应③的反应类型是 。在一定条件下,化合物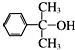 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ,Ⅴ的结构简式是 。
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ,Ⅴ的结构简式是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
等物质的量的下列物质,分别完全燃烧时,消耗氧气最少的是
A.苯 B.甲烷 C.乙烯 D.乙醇
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三高考考前模拟十二化学试卷(解析版) 题型:推断题
聚合物G可用于生产全生物降解塑料,在“白色污染”日益严重的今天有着重要的作用.有关转化关系如下:

已知:CH3CH2CH2Br→+NaOHCH3CH2CH2OH+NaBr,淀粉在硫酸催化下水解生成葡萄糖.
请回答下列问题:
(1)物质A的分子式为__________,B的结构简式为_____________。
(2)F中含氧官能团的名称________。
(3)反应①~④中属于加成反应的是________。
(4)写出由两分子F合成六元环化合物的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三高考考前模拟十二化学试卷(解析版) 题型:选择题
某溶液中可能含有物质的量浓度相等的下列离子中的几种:Fe3+、Cu2+、Na+、SO42-、CO32-、NO3-、Cl-、I-,取上述溶液少量分别进行如下实验:①一份中加入少量锌粉后,固体溶解、溶液颜色有变化,但无其它现象产生②一份加入BaCl2溶液后得到白色沉淀,下列有关判断正确的是( )
A.溶液中只含Fe3+、SO42-、Cl-
B.溶液中只含Cu2+、SO42-
C.需要利用焰色反应才能确定有无Na+
D.溶液中肯定没有I-,但无法确定有无Cl-
查看答案和解析>>
科目:高中化学 来源:2016届江西省、临川二中高三下联考理综化学试卷(解析版) 题型:简答题
(1)甲醇是重要的可再生燃料。已知在常温常压下:
2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(g) ΔH=-1275.6 kJ/mol
2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ/mol
H2O(g)===H2O(l) ΔH=-44.0 kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为__________。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g) 2NH3(g)反应的影响。实验结果如图所示:
2NH3(g)反应的影响。实验结果如图所示:

(图中T表示温度,n表示物质的量)
①比较在a、b、c三点N2 的转化率最高的是 (填字母).
②在起始体系中加入N2的物质的量为 mol时,反应后氨的百分含量最大,若容器容积为1L,n=3mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K= 。(保留3位有效数字)
(3)古代铁器(埋藏在地下)在严重缺氧的环境中,仍然锈蚀严重(电化学腐蚀)。原因是一种叫做硫酸盐还原菌的细菌,能提供正极反应的催化剂,每48gSO放电转移电子数为2.408×1024,该反应放出的能量供给细菌生长、繁殖之需。
①写出该电化学腐蚀的正极反应的电极反应式:
②文物出土前,铁器表面的腐蚀产物可能有(写化学式)
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5mol/L100mLFeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入_______mL、2mol/L的盐酸(总体积忽略加入盐酸体积)。
查看答案和解析>>
科目:高中化学 来源:2016届江西省、临川二中高三下联考理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.25℃时,50 g 98%浓硫酸和50 g 98%浓磷酸混合后含氧原子数为4NA
B.28 g聚乙烯中含有的碳原子数为2n NA
C.常温常压下,0.2 g D216O中含有的质子数、中子数和电子数均为0.1NA
D.6.8 g KHSO4晶体中含有0.1 NA个阳离子
查看答案和解析>>
科目:高中化学 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:填空题
甲醇是重要的化工原料,又可称为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)═CH3OH(g)△H
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-58kJ·mol-1
③CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ·mol-1
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
化学键 | H-H | C-O |
| H-O | C-H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | x |
则x=__________。
(2)若T℃时将6molCO2和 8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间的变化如图中状态Ⅰ(图中实线)所示。图中数据A(1,6)代表在1min时H2的物质的量是6mol。
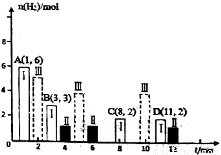
①T℃时状态I条件下,0--3min内CH3OH的平均反应速率v=__________(保留两位有效数字),
平衡常数K=__________;
②其他条件不变时,仅改变某一条件后测得H2的物质的量随时间变化如图中状态Ⅱ所示,则改变的条件可能是__________。
③一定温度下,此反应在恒容容器中进行,能判断该反应达到化学平衡状态依据的是__________
a.容器中压强不变
b. CO2和水蒸气的体积比保持不变
c. v正(H2) =3v逆(CH3OH )
d.气体的密度不再随时间的改变而变化
④CO与H2在密闭容器中发生反应①,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示。下列说法正确的是__________
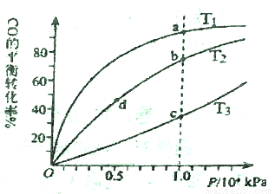
A.温度:T1<T2<T3
B.正反应速率:v(a)>v(c);v(b)>v(d)
C.平衡常数:K(a)>K(c);K(b)>K(d)
D.平均摩尔质量:M(a)<M(c);M(b)>M(d)
⑤800K向下列起始体积相同的密闭容器中充入1molCO、2molH2发生反应①,如图所示甲容器在反应过程中保持压强不变,乙容器保持体积不变达到平衡时H2的浓度c (H2)甲__________c(H2)乙
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:填空题
化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素原子最外层的p轨道中的电子数等于前一电子层的电子总数,X原子最外层的p轨道中有一个轨道填充了2个电子。
(1)X原子的电子排布式是____________,Y原子的价层电子排布图是: 。
(2)YX2的立体构型是________,YX2的熔、沸点比ZX2________(填“高”或“低”)。
(3)YX2分子中,Y原子的杂化类型是________,一个YX2分子中含________个π键。
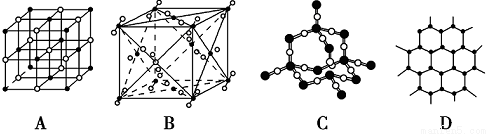
(4)下图表示一些晶体的结构(晶胞),其中代表YX2的是________,代表ZX2的是________(填序号,下同)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com