
分析 等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4 mol/L,混合后c(CO32-)=$\frac{2×1{0}^{-4}mol/L}{2}$=1×10-4 mol/L,结合Ksp计算.
解答 解:等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4 mol/L,混合后c(CO32-)=$\frac{2×1{0}^{-4}mol/L}{2}$=1×10-4 mol/L,Ksp=2.8×10-9,则混合后c(Ca2+)=$\frac{2.8×1{0}^{-9}}{1×1{0}^{-4}}$=2.810-5mol/L,则生成沉淀所需CaCl2溶液的最小浓度为$\frac{2.8×1{0}^{-5}mol/L}{\frac{1}{2}}$=5.6×10-5mol/L,
故答案为:5.6×10-5mol/L.
点评 本题考查难溶电解质及Ksp计算,为高频考点,把握Ksp与离子浓度的关系为解答的关键,侧重分析与计算能力的考查,注意等体积混合前后离子浓度的变化,题目难度不大.


 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 氨水可使酚酞试剂变为红色,说明氨溶解于水显弱碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯分子有8个σ键,1 个π键 | B. | 丙烯分子中3个碳原子都是sp3杂化 | ||
| C. | 丙烯分子不存在非极性键 | D. | 丙烯分子中所有原子都共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
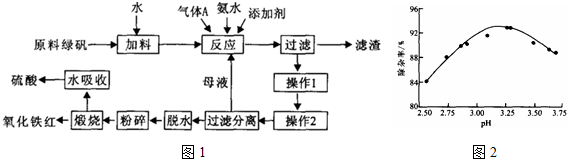
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热△H=-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 一定条件下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 在101 kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| D. | HCl和NaOH反应的中和热△H,则相同温度下H2SO4和Ca(OH)2反应的热效应2△H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时金属锂作负极 | B. | 放电时OH-向正极移动 | ||
| C. | 水既是氧化剂又是溶剂 | D. | 总反应为:2Li+2H2O=2LiOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
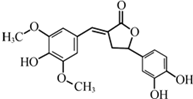
| A. | 分子中含有三种含氧官能团 | |
| B. | 既能与FeC13发生显色反应,也能和Na2CO3反应 | |
| C. | 既可以发生取代反应,又能够发生加成反应 | |
| D. | 1 mol该化合物最多能与6molNaOH反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com