
下列实验中,颜色的变化与氧化还原反应无关的是
A.SO2使酸性KMnO4溶液褪色
B.Na2O2投入酚酞溶液中溶液先变红后褪色
C.向FeSO4溶液中滴NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色
D.往紫色石蕊试液中通入氨气,溶液变蓝
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列反应中,属于取代反应的是( )
①CH3CH=CH2+Br2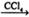 CH3CHBrCH2Br ②CH3CH2OH
CH3CHBrCH2Br ②CH3CH2OH 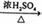 CH2=CH2+H2O
CH2=CH2+H2O
③CH3COOH+CH3CH2OH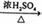 CH3COOCH2CH3+H2O ④2CH3CH2OH
CH3COOCH2CH3+H2O ④2CH3CH2OH 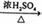 CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
A. ①② B.③④ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
通式为CnH2n-2的一种气态烃完全燃烧后生成CO2和H2O的物质的量之比为4:3,这种烃的链状同分异构体有( )
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D、E、F、G七种位于周期表前四周期元素,其原子序数依次增大,相关信息如下表所示:
| 元素 | 性质 |
| A | 一种核素的原子核内不含中子 |
| B | 原子核外电子有6种不同运动状态 |
| C | 最高价氧化物的水化物与其氢化物可发生非氧化还原反应 |
| D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
| E | 在地壳中的含量位居第三 |
| F | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
| G | 该元素的一种氧化物M可用作油漆颜料,与E的单质反应可应用于焊接钢轨 |
根据以上信息,回答下列问题:
⑴ 画出元素C的基态原子核外电子排布图: ;G元素位于周期表的 区;
B、C、D三种元素的第一电离能由大到小顺序为: (用元素符号表示)。
⑵ 化合物BA2D2蒸气293 K时,理论测算密度为2.0g·L-1,实际密度为2.5 g·L-1的原因是 。
⑶ FD2中F原子的杂化类型为 ;分子空间构型为 ;FD2易溶于水的原因可能是: (填入序号)。
①FD2与水极性相同 ②FD2可以与水反应
⑷ 有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为:
查看答案和解析>>
科目:高中化学 来源: 题型:
丁烷广泛应用于家用液化石油气,也用于打火机中作燃料,下列关于丁烷的叙述中不正确的是
A.C4H10与C(CH3)4互为同系物
B.正丁烷分子中四个碳原子排列成一条直线
C.丁烷在常温下是气体
D.C4H10进行一氯取代后可生成四种沸点不同的有机产物
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组的同学利用下列装置进行乙醇催化氧化的实验。请分析回答:
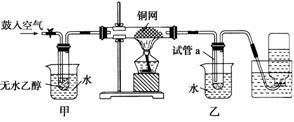

(1)请写出实验过程中的总的化学反应方程式______________________________。
(2)在不断鼓入空气的情况下,移去酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是________反应。进一步研究表明,鼓气速度与反应体系的温度关系曲线如右图所示。鼓气速度过快,反应体系温度反而下降的原因___________________________。
(3)甲和乙两个水浴作用不相同。
甲的作用是________________;乙的作用是_________________________。
(4)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是___________。
集气瓶中收集到的气体的主要成分是_______________。
(5)在检验生成物的过程中,一位同学很偶然地发现向溴水中加入乙醛溶液,溴水褪色。针对溴水褪色的原因,该小组的同学们经过分析后,提出两种猜想:
①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应。
请你设计一个简单的实验,探究哪一种猜想正确?__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
钛合金被誉为二十一世纪的金属,具有广泛的用途。金属钛可用下列方法提炼:
① TiO2+2C+2Cl2 TiCl4+2CO ② TiCl4+2Mg
TiCl4+2CO ② TiCl4+2Mg 2MgCl2+Ti
2MgCl2+Ti
对上述两个反应,下列有关叙述正确的是
A.反应①中碳元素被还原 B.反应②中钛元素被氧化
C.反应①中Cl2是还原剂 D.反应②中TiCl4是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,向密闭容器中充入1.0molN2和3.0molH2,反应达到平衡时测得NH3的物质的量为0.6mol。若在该容器中开始时充入2.0 molN2和6.0molH2,则平衡时NH3的物质的量 ( )
A、若为定容容器,n(NH3)=1.2mol B、若为定容容器,n(NH3)>1.2mol
C、若为定压容器,n(NH3) >1.2mol D、若为定压容器,n(NH3)<1.2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com