
http://www..com/11反应N2O4(g) ![]() 2NO2(g);ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g);ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
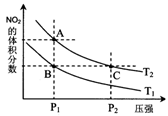
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
科目:高中化学 来源: 题型:
目前燃料电池中能量转化效率最高的是陶瓷电池,此类电池正面涂有黑色的稀有金属复合氧化物,作为正极,反面是一层较厚的绿色“金属陶瓷”,作为负极。在750℃实验温度下,空气中的氧分子吸附于黑色正极,氧原子会分别从涂层中“抢走”2个电子,变成氧离子,随后氧离子穿过陶瓷膜,与负极那一边的燃气反应,并释放出能量,氧不断“劫持”电子穿越薄膜,正负两极间便形成电压,产生电流。
(1)水煤气成分是 。水煤气又称为合成气,在一定条件下可以合成二甲基醚时,还产生一种可以参与大气循环的无机化合物,写出该化学方程式可能是 。
http://www..com/(2)若以水煤气为上述陶瓷电池的燃料气,则电池的负极反应方程式为 。
(3)下图是丙烷、二甲醚燃烧过程中能量变化图,w.w.w.k.&s.5*u.c.om
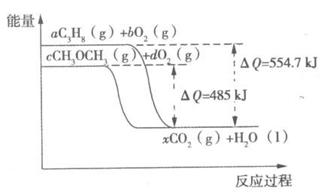
其中x为各自反应中对应的系数。根据该图写出二甲醚燃烧的热化学方程式
若以第⑵问中陶瓷电池为电源,用惰性电极电解硝酸银溶液,为保证阴极有 10.8g银析出,试求制备水煤气时![]() , 至少需要碳 g
, 至少需要碳 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com