
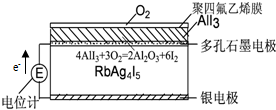
| A. | 电子从银电极在RbAg4I5晶体中迁移流向石墨电极 | |
| B. | Ag+从下往上移动 | |
| C. | 石墨电极为正极,银电极为负极 | |
| D. | 银电极的电极反应是:Ag-e-=Ag+ |
分析 Ag和I2作用形成原电池,生成物为RbAg4I5,可知在反应中Ag被氧化,为电池的负极反应,I2被还原,为原电池的正极反应,原电池工作时,阳离子向正极移动,阴离子向负极移动.
解答 解:Ag和I2作用形成原电池,生成物为RbAg4I5,可知在反应中Ag被氧化为电池的负极反应,I2被还原,为原电池的正极反应,则:
A.反应后I2→I-,I2被还原,为原电池的正极反应,银为电池的负极,电子从负极流向正极,即由银电极沿外电路流向石墨电极,故A错误;
B.原电池工作时,阳离子向原电池正极移动,Ag+从下往上移动,故B正确;
C.石墨电极为正极,银电极为负极,故C正确;
D.Ag被氧化,为电池的负极反应,银电极的电极反应是:Ag-e-=Ag+,故D正确.
故选:A.
点评 本题考查原电池反应,题目难度中等,注意根据生成物判断原电池的正负极,为解答该题的关键,注意原电池的正负极的判断,把握电极反应式的书写.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:多选题
| A. | 氢氧化钡溶液与盐酸反应:OH-+H+=H2O | |
| B. | 向 FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl- | |
| C. | 小苏打溶液与烧碱溶液反应:HCO3-+OH-=CO32-+H2O | |
| D. | 氯气通入冷水中:Cl2+H2O=Cl-+ClO-+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧杯 | B. | 漏斗 | C. | 玻璃棒 | D. | 胶头滴管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:3:5 | B. | 2:5:5 | C. | 2:1:5 | D. | 2:2:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

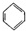 +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$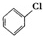 +HCl
+HCl| 项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
| 苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是铵盐均能与苛性钠共热产生氨气 | |
| B. | 向铜粉中加人稀硫酸,铜粉不溶解;再加人Cu(NO3)2固体,铜粉溶解 | |
| C. | 普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高 | |
| D. | 将二氧化硫通人溴水,溴水褪色后加热不能恢复原色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com