


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.某无色无味气体通入澄清石灰水中,石灰水变浑浊,则该气体为CO2 |
| B.某气体能使湿润的红色石蕊试纸变蓝,则该气体水溶液显碱性 |
| C.某无色溶液中加入盐酸酸化的BaCl2溶液,产生白色沉淀,则该溶液中一定有SO42- |
| D.用可见光束照射某红褐色液体产生丁达尔现象,则该液体为胶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
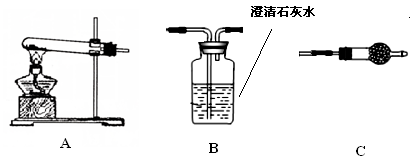
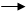
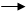 (1)各装置连接顺序为 。
(1)各装置连接顺序为 。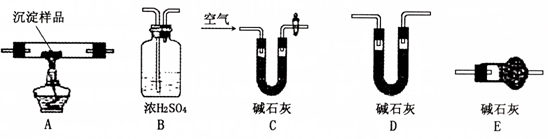
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
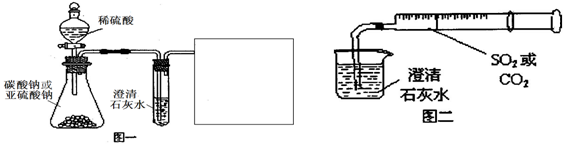
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| A.氯化钠溶液 | B.苯 | C.碳酸氢钠溶液 | D.四氯化碳 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.浓盐酸附近产生白烟:NH3与HCl气体反应产生了NH4C1固体 |
| B.浓硫酸附近无明显现象:NH3与浓硫酸不发生反应 |
| C.氯化物溶液变浑浊:该溶液一定是A1Cl3溶液 |
| D.湿润的红色石蕊试纸变蓝:NH3的水溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
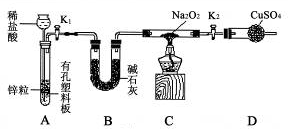
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
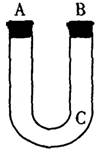
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碱式滴定管用蒸馏水洗净后,直接加入未知浓度的NaOH溶液 |
| B.锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液 |
| C.滴定前,没有逐出酸式滴定管尖嘴处的气泡,滴定终点时气泡消失 |
| D.滴定前读数正确,达到滴定终点后,俯视读数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com