
| A. | 12.5g | B. | 10.5g | C. | 13.2g | D. | 24.4g |
分析 CH4燃烧产物为CO、CO2、H2O(g),产物通过无水CaCl2时,无水CaCl2的作用是吸收水分,无水CaCl2增重25.2g为水的质量,根据H原子守恒可计算CH4的物质的量,根据C原子守恒可计算CO和CO2的总的物质的量,再根据二者质量可计算CO2的物质的量,进而计算CO2质量.
解答 解:产物通过无水CaCl2时,无水CaCl2增重25.2g为水的质量,
所以n(H2O)=$\frac{25.2g}{18g/mol}$=1.4mol,
根据H原子守恒,可知:n(CH4)=$\frac{1}{2}$n(H2O)=$\frac{1}{2}$×1.4mol=0.7mol,
根据C原子守恒,则:n(CO)+n(CO2)=0.7mol,
燃烧生成一氧化碳、二氧化碳的质量为:m(CO)+m(CO2)=49.6g-25.2g=24.4g,
所以[0.7mol-n(CO2)]×28g/mol+n(CO2)×44g/mol=24.4g,
解得:n(CO2)=0.3mol,
所以生成二氧化碳的质量为:0.3mol×44g/mol=13.2g,
故选C.
点评 本题考查化学计算,题目难度不大,注意从原子守恒的角度解答,关键根据水的质量判断甲烷的物质的量,试题培养了学生的分析能力及化学计算能力.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:选择题
| A. | NO2的消耗速率与NO的生成速率相等 | |
| B. | 容器内压强不随时间变化而变化 | |
| C. | NO2和O2的消耗速率之比为1:1 | |
| D. | 单位时间内生成2n mol NO.同时生成n mol O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | mol/L•s | B. | mol•(L•min)-1 | C. | mol/(L•min) | D. | mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极的电极反应式为:CH4+10OH--8e-═CO32-+7H2O | |
| B. | 通入氧气的一极发生氧化反应,通入甲烷的一极发生还原反应 | |
| C. | 随着反应的进行,电解质溶液的pH增大 | |
| D. | 甲烷燃料电池的能量利用率比甲烷燃烧的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
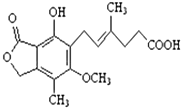 麦考酚酸是一种有效的免疫抑制剂,能有效地防止肾移植排斥,其结构简式如图所示.下列有关麦考酚酸说法不正确的是( )
麦考酚酸是一种有效的免疫抑制剂,能有效地防止肾移植排斥,其结构简式如图所示.下列有关麦考酚酸说法不正确的是( )| A. | 分子式为C17H22O6 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 1mol麦考酚酸最多能与3mol NaOH反应 | |
| D. | 1mol麦考酚酸最多能与4mol H2发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com