
��1����Ԫ���ж��ֻ��ϼۣ����γɶ��ֻ������д�±��еĿհף�
|
���ϼ� |
-2 |
-1 |
0 |
+2 |
+4 |
+6 |
+7 |
|
������Ļ�ѧʽ |
|
FeS2 |
S |
Na2S2O3 |
|
SO3��H2SO4��Na2SO4 |
Na2S2O8 |
��2����֪NaHSO3��Һ������ݣ���д������Һ�д��ڵĸ���ƽ�ⷴӦ�����ӷ���ʽ�� ��
��3���밴��Ũ���ɴ�С��˳������Na2SO3��Һ�е����ӣ� ��
Na2SO3��Һ�����ڿ�����һ��ʱ�����Һ��pH (�������С�����䡱)��(������ˮ������)ԭ����
��
��4��ijͬѧ�������ʵ������̽��Na2S2O3�Ļ�ѧ���ʡ�
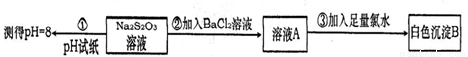
ʵ��ٿ�˵��Na2S2O3�ܷ���ˮ�⣬ʵ��ڢ�˵��Na2S2O3���� �ԡ�����Ԥ��Na2S2O3�����ܾ��еĻ�ѧ����(�о�2������) �� ��
��1����2�֣�
|
���ϼ� |
-2 |
-1 |
0 |
+2 |
+4 |
+6 |
+7 |
|
������Ļ�ѧʽ |
Na2S��H2S�� |
|
|
|
SO2��Na2SO3 |
|
|
��2��HSO3��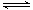 H��+SO32����HSO3��+H2O
H��+SO32����HSO3��+H2O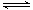 H2SO3+OH����H2O
H2SO3+OH����H2O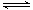 H��+OH������3�֣�ÿ������ʽ1�֣�
H��+OH������3�֣�ÿ������ʽ1�֣�
��3��c��Na������c��SO32������c��OH������c��HSO3������c��H������2�֣�����С��1�֣���2SO32����O2=2SO42����SO32������������SO42����SO32����Ũ�ȼ�С��ˮ�������OH��Ũ�ȼ�С����ҺpH��С����2�֣�ֻҪ������������д����ʽҲ�÷֣�
��4����ԭ�����������ԡ������ԣ������������ӽ�ϲ���������������ԣ������γ��������ܷ����绯��Ӧ����Ⱦ����������־��л�ԭ�ԣ��������һ��1�֣���3�֣����÷֣�ֻҪ�������ɵ÷֣�
��������
�����������1����Ԫ�ر���-2�ۣ������Ƶȣ���Ԫ�ر���+4�ۣ��ж��������������εȣ��ʴ�Ϊ��Na2S�ȣ�SO2�ȣ�
��2����Һ�д���ˮ�ĵ���ƽ�⡢����������ĵ���ƽ����ˮ��ƽ�⣬ƽ�ⷴӦ�����ӷ���ʽ�ֱ�ΪHSO3��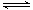 H��+SO32����HSO3��+H2O
H��+SO32����HSO3��+H2O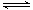 H2SO3+OH����H2O
H2SO3+OH����H2O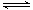 H��+OH����
H��+OH����
��3��Na2SO3��Һ�������ˮ��õ��������������Һ�ʼ��ԣ�����������ˮ��õ������ᣬͬʱ����ˮ�ĵ��룬����Һ�����������ӵ�Ũ�ȴ���������������ӣ����������£�������Ũ��ԭС���������������Ũ�ȣ�ˮ��̶Ȳ����������Ũ�ȴ�������������Ũ�ȣ�����Һ������Ũ�ȴ�С��ϵΪ��c��Na������c��SO32������c��OH������c��HSO3������c��H������
Na2SO3��Һ�����ڿ�����һ��ʱ���SO32������������SO42����SO32����Ũ�ȼ�С��ˮ�������OH��Ũ�ȼ�С����ҺpH��С��
��4��Na2S2O3��Һ���Ȼ�����Һ��Ϻ�û��������������ˮ���а�ɫ�������ɣ��ó���Ϊ���ᱵ����Ӧ����Ԫ�صĻ��ϼ����ߣ�Na2S2O3���ֻ�ԭ�ԣ�
Na2S2O3����Ԫ�صĻ��ϼ۴����м��̬�����������ԡ���ԭ�ԣ����ܷ����绯��Ӧ�ȣ�
���㣺���⿼����Ԫ�ػ���������ʡ����û�ѧ�������ˮ�⡢����Ũ�ȱȽϵȡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ���ݷ�ˮ�������к����ʵIJ�ͬ����ҵ���ж��ַ�ˮ�Ĵ���������
���ݷ�ˮ�������к����ʵIJ�ͬ����ҵ���ж��ַ�ˮ�Ĵ���������| 8000��(15-cV2) |
| V1 |
| 8000��(15-cV2) |
| V1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���ϼ� | -2 | -1 | 0 | +2 | +4 | +6 | +7 |
| ������Ļ�ѧʽ | Na2S�� Na2S�� |
FeS2 | S | Na2S2O3 | SO2�� SO2�� |
SO3��H2SO4��Na2SO4 | Na2S2O8 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| 8000��(15-cV2) |
| V1 |
| 8000��(15-cV2) |
| V1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�������и�����ѧ��12���¿����ۻ�ѧ�Ծ��������棩 ���ͣ������
��Ԫ���ж��ֻ��ϼۣ����γɶ��ֻ����
��1����������1 mol��L��1 100 mL NaOH��Һǡ����ȫ����0.1 mol SO2���壬�˷�Ӧ�����ӷ���ʽΪ ������ҺpH_______7(�=����>������)��
��2��ijͬѧ�ڳ������������ʵ������̽��Na2S2O3�Ļ�ѧ���ʡ�

ʵ��ٿ�˵��________(����ĸ)
A����Na2S2O3��Һ��ˮ�����c(OH��)=10��8mol/L
B��H2S2O3��һ������
C��Na2S2O3��һ���������
D��Na2S2O3ˮ�ⷽ��ʽΪS2O32��+2H2O=H2S2O3+2OH��
д��ʵ��ڷ�����Ӧ�����ӷ���ʽ ��
��3��ʵ�����Ƶõ�Na2S2O3�־��������������������ʡ�Ϊ�˲ⶨ�ֲ�Ʒ��Na2S2O3��5H2O(Ħ������Ϊ248g/mol)�ĺ�����һ�������������������KMnO4��Һ�ζ��ķ���(�ٶ��ֲ�Ʒ������������KMnO4��Һ����Ӧ)����ȡ1.28 g�Ĵ���Ʒ����ˮ����0.40mol/L KMnO4��Һ(�������������ữ)�ζ�������Һ��S2O32��ȫ��������ʱ������KMnO4��Һ���20.00 mL��(��֪��5S2O32��+8MnO4��+14H+=8Mn2++10SO42��+7H2O)��
�Իش�
��KMnO4��Һ���ڡ���(���ʽ����ʽ��)�ζ����У��ζ��յ������Ϊ ��
�����ζ�ʱ����֣��տ�����Һ�ֲ���ɫ��ֹͣ�ζ������ʹ��Ʒ��Na2S2O3��5H2O�����������IJ������_____________(�ƫ�ߡ���ƫ�͡����䡱)��
�۲�Ʒ��Na2S2O3��5H2O����������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�긣��ʡ�����б�ҵ������������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ֵ�����ܶ࣬����һ����Ԫ�����⣬�����н϶��Cr(������Ni(������Mo(�⣩������ ��Si(�裩��C(̼��������S(��P(�ף���
��1������Ԫ�������ڵ��������ҵ�һ�����ܴӴ�С���е���_______
��2��Mo���⣩���ڵ������ڣ�����Cr������Ԫ��λ��ͬһ�壬���̬Mo���⣩ԭ�ӵ���Χ���ӣ��۵��ӣ��Ų�ʽ��_______��
��3��CH4�ķе��SiH4�ͣ�ԭ����_______��
��4����Ԫ�����γɶ�������������[Ni(CN)4]2���в����е���____����ѡ���ţ���
A�����Ӽ� B����λ�� C���Ҽ� D���м� E�����
��5��̼Ԫ���ж��ֵ��ʣ�����C60�����ж��ص����νṹ��C60������ԭ�ӹ���ӻ�������_______��

��6��̼����һ�ֵ���ʯī�ʲ�״�ṹ����һ̼þ���Ͳ��Ͼ�����ʯī̼ԭ�Ӳ�����þԭ�Ӳ㣬���㸩��ͼ��

�ò��ϵĻ�ѧʽΪ_______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com