
����Ŀ�����к�NaCl��Na2SO4��NaNO3�Ļ���ѡ���ʵ����Լ�����ת��Ϊ��Ӧ�ij�������壬�Ӷ�ʵ��Cl-��SO42-����NO3-������롣��Ӧ��ʵ����̿�����ͼ��ʾ��
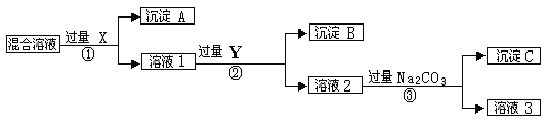
��ش��������⣺
��1��д��ʵ���������������ʵĻ�ѧʽ���Լ�X �� ������A�� ���Լ�Y�� ������B�� ��
��2������ʵ�������м��������Na2CO3��Ŀ���� ��
��3������ʵ�鷽���õ�����Һ3�п϶����� (�ѧʽ)���ʣ�Ϊ�˽��������⣬��������Һ3�м��������� ��֮����Ҫ��ù���NaNO3����е�ʵ������� (���������)��
���𰸡�
��1��BaCl2��Ba(NO3)2��BaSO4��AgNO3��AgCl����4�֣�
��2��ʹ��Һ�е�Ag+��Ba2+��ȫ��������3�֣�
��3��Na2CO3��ϡHNO3��������3����
����������1��ʵ���ҷ��뺬NaCl��Na2SO4��NaNO3�Ļ������ʵ��Cl-��SO42-����NO3-������������ڻ�����м���BaCl2��Ba(NO3)2������BaSO4������������ӦΪBa2++SO42-=BaSO4����Ȼ����������AgNO3����AgCl��������Ӧ�����ӷ���ʽΪCl-+Ag+=AgCl�����ʴ�Ϊ��BaCl2��Ba(NO3)2��BaSO4��AgNO3��AgCl��
��2�������������Na2CO3��ʹ��Һ�е�Ag+��Ba2+��ȫ����������֮��������ϡHNO3��Һ�Ӷ��õ�NaNO3���ʴ�Ϊ��ʹ��Һ�е�Ag+��Ba2+��ȫ������
��3�����������Na2CO3����ʵ�鷽���õ�����Һ3�п϶�����Na2CO3��Na2CO3��ϡHNO3��Һ��Ӧ���ɶ�����̼�����NaNO3��������ɵõ�NaNO3���ʴ�Ϊ��Na2CO3��ϡHNO3��������


 ����ʦ���һ��һ��ϵ�д�
����ʦ���һ��һ��ϵ�д� �Ͻ�ƽ��У����ϵ�д�
�Ͻ�ƽ��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��µĺ���������,���������������ٷ����仯ʱ,����������ӦA��s�� +3B��g��![]() 2C��g��+D��g���Ѵ�ƽ��״̬����������ֻ��B��������ɫ��
2C��g��+D��g���Ѵ�ƽ��״̬����������ֻ��B��������ɫ��
A����������ѹǿ
B�����������ܶ�
C�������ƽ��������
D���������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ���³�ѹ�£�1mol CH4�������22.4L
B. 1molFe����������ȫȼ��ʧȥ������Ϊ2NA
C. �ü��������ɼ���Fe(OH)3�����FeCl3��Һ
D. ����ɫ��Ӧ�ɼ���NaCl��Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ɫ����ζ��������(����)
A. Cl2 B. SO2 C. N2 D. NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ԫ��H2A��ˮ�д������µ��룺H2A==H++HA-��HA-![]() H++A2-���ش��������⣺
H++A2-���ش��������⣺
��1��Na2A��Һ��________�ԣ�������___________�������ӷ���ʽ��ʾ����
��2��NaHA��Һ��________�ԣ�������___________��
��3��0.1mol/L��NaHA��Һ��PH=3����Ka(HA-)=_____________��
��4��ij�¶��£���10 mL 0.1 mol/L NaHA��Һ�м���0.1 mol/L KOH��ҺV mL����Һ��ˮ�����ӻ�����Ka=c2(OH-)����ʱ��Һ��___________�ԣ�V____________10 �������������������c(K+)/c(Na+) ____________1�����������������������Һ�е���غ��ʽΪ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶�����������þ������Һ�д������¹�ϵ��c��Mg2������c2��OH������Ksp�����ƶ�������þ��������Һ�е��ܽ���ɴ�С��˳����
��0��1mol��L��1��AlCl3��Һ��0��1mol��L��1��NH4Cl��Һ
��0��1mol��L��1��KCl��Һ��0��1mol��L��1��KAlO2��Һ
A���٢ܢۢ�
B���٢ڢۢ�
C���ۢ٢ܢ�
D���ܢ٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������2009��12���ڵ������籾ɶ���ٿ�������2012����2020��ȫ�������������Э�顣�����������������������
A��N2 B��H2 C��CO2 D��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������X��Һ�ֱ�����ĸ�ʢ��10mL 2mol/L������ձ��У�����ˮϡ�͵�50mL����ʱX������ͻ��ؽ��з�Ӧ�����з�Ӧ���������ǣ� ��
A.20mL 3mol/L ��X��Һ
B.20mL 2mol/L ��X��Һ
C.10mL 4mol/L��X��Һ
D.10mL 2mol/L��X��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����������ų�����(����)
A. �Ͽ������е�H��H��
B. Ba(OH)2��8H2O������NH4Cl���巴Ӧ
C. C��H2O(g)��Ӧ
D. Zn��ϡH2SO4��Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com