
用0.102 6 mol·L-1的盐酸滴定25.00 mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如下图所示,正确的读数为( )

A.22.30 mLB.22.35 mLC.23.65 mLD.23.70 mL
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源:2014年高二化学人教版选修四 20燃料电池练习卷(解析版) 题型:填空题
可以将氧化还原反应2H2+O2 2H2O设计成原电池。
2H2O设计成原电池。
(1)利用氢气和氧气、氢氧化钾溶液构成燃料电池,则负极通的气体应是 ,正极通的气体就是 ,电极反应为:正极 ,负极 。
(2)如果把KOH改为稀硫酸作电解质,则电极反应为:正极: ,负极: 。
(3)(1)和(2)的电解质溶液不同,反应进行后,其溶液的pH各有何变化? 。
(4)如把H2改为甲烷,KOH溶液作电解质溶液,则电极反应为:正极: ,负极: 。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 17难溶电解质的溶解平衡练习卷(解析版) 题型:选择题
某温度时,BaSO4在水中的沉淀溶解平衡曲线如下图所示。下列说法正确的是( )
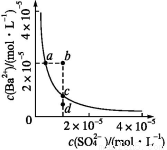
提示:BaSO4(s)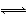 Ba2+(aq)+S(aq)的平衡常数Ksp=c(Ba2+)·c(S),称为溶度积常数。
Ba2+(aq)+S(aq)的平衡常数Ksp=c(Ba2+)·c(S),称为溶度积常数。
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 15盐类水解的原理练习卷(解析版) 题型:填空题
(1)浓度均为0.01 mol·L-1的8种溶液:①HNO3 ②H2SO4 ③CH3COOH ④Ba(OH)2 ⑤NaOH
⑥CH3COONa ⑦KCl ⑧NH4Cl,这些溶液pH由小到大的顺序是(填写编号) 。
(2)pH=2的某酸HnA(An+为酸根)与pH=12的某碱B(OH)m混合,恰好反应生成正盐,混合液pH=8。
①反应生成的正盐的化学式为 。
②该盐中 离子一定能水解,其第一步水解的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 15盐类水解的原理练习卷(解析版) 题型:选择题
关于盐类水解的实质,下列叙述正确的是( )
A.盐的电离平衡被破坏B.水的电离平衡被破坏
C.没有中和反应发生D.溶液的pH一定变大
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 14酸碱中和滴定练习卷(解析版) 题型:选择题
酸碱恰好完全中和时( )
A.酸与碱的物质的量一定相等
B.溶液呈现中性
C.酸与碱的物质的量浓度相等
D.酸所能提供的H+与碱所能提供的OH-的物质的量相等
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 13pH的计算练习卷(解析版) 题型:选择题
常温下,柠檬酸水溶液的pH是3,食用醋的pH是2,可乐的pH是6,三种物质的溶液中c(OH-)分别是( )
A.1×10-11 mol·L-1,1×10-12 mol·L-1,1×10-8 mol·L-1
B.1×10-11 mol·L-1,1×10-8 mol·L-1,1×10-12 mol·L-1
C.2×10-11 mol·L-1,1×10-10 mol·L-1,1×10-8 mol·L-1
D.1×10-8 mol·L-1,1×10-11 mol·L-1,1×10-12 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 11弱电解质的电离练习卷(解析版) 题型:选择题
一元弱酸HA(aq)中存在下列电离平衡:HA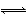 A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
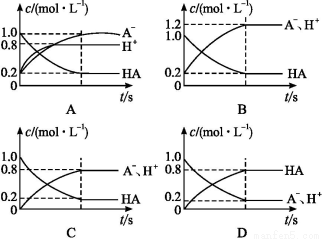
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修二 4.2 表面活性剂精细化学品练习卷(解析版) 题型:填空题
洗衣粉的主要成分之一是烷基苯磺酸钠,常用的是十二烷基苯磺酸钠,其合成路线如下:
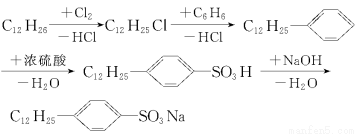
请回答下列问题:
(1) 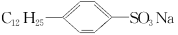 分子中的亲水基是__________,亲油基是__________。
分子中的亲水基是__________,亲油基是__________。
(2)由十二烷基苯制取十二烷基苯磺酸的化学方程式为___________,反应类型为___________________。
(3)用油脂可以制肥皂,从硬脂酸甘油酯生成硬脂酸钠和甘油的化学方程式为________________________________,反应类型为________________________。
(4)在洗涤剂中添加酶制剂能促进污垢中的蛋白质(如奶渍、肉汤)等水解为可溶性的物质而被除去。使用加酶洗衣粉的水溶液中浸泡10~30 min,水温在40~50 ℃最佳。加酶洗衣粉不宜在高温、潮湿环境中贮存,也不宜久存。为什么?
__________________________________________________________。
(5)过去使用的合成洗涤剂中常加入三聚磷酸钠(Na5P3O10)作助剂,它可使硬度大的洗涤水软化,对微细的无机粒子或油脂具有分散、乳化、胶溶作用,防止污渍再次沉积到衣物上;它还能维持水溶液的弱碱性,提高洗涤剂的去污能力和洗涤效果。但是,20世纪90年代以来,世界各国先后提出必须生产和使用无磷洗涤剂。请解释原因______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com