
分析 根据n=$\frac{V}{{V}_{m}}$计算混合气体的物质的量,令混合气体中CO和CO2的物质的量分别为xmol、ymol,根据二者质量之和与物质的量之和列放出计算x、y的值,再根据V=nVm计算CO的体积,根据m=nM计算CO2的质量.
解答 解:标准状况下,混合气体的物质的量为$\frac{20.16L}{22.4L/mol}$=0.9mol,
令混合气体中CO和CO2的物质的量分别为xmol、ymol,则:
$\left\{\begin{array}{l}{x+y=0.9}\\{28x+44y=36}\end{array}\right.$
解得:x=0.225,y=0.675;
则CO所占的体积为:22.4L/mol×0.225mol=5.04L;
CO2的质量为:0.675mol×44g/mol=29.7g;
故答案为:5.04;29.7.
点评 本题考查物质的量的有关计算、混合物的有关计算等,比较基础,注意对基础知识的理解掌握,注意对公式的理解与运用.


科目:高中化学 来源: 题型:推断题
| 周期\族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ①③⑤ | C. | ②④⑥ | D. | ③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
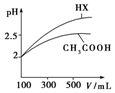 25℃时部分弱电解质的电离平衡常数数据如表所示:
25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| B. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶内的液面以下 | |
| C. | 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 用滴管滴加液体时滴管应垂直悬垂在容器上方且不能触及容器内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
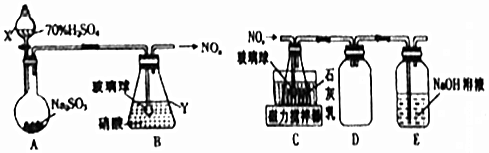
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com