
分析 (1)pH=a的强酸加水稀释至原来体积的10b倍,则溶液的pH变为a+b(当a+b>7时,让pH=7);
(2)pH=a的强酸加水稀释至原来体积的10b倍,则溶液的pH变为a+b(当a+b>7时,让pH=7);
(3)pH=a的弱酸加水稀释至原来体积的10b倍时,则溶液的pH<a+b,因为加水促进了弱电解质的电离.
解答 解:(1)pH=a的强酸加水稀释至原来体积的10b倍,则溶液的pH变为a+b(当a+b>7时,让pH=7),故将pH=1的盐酸加水稀释至100倍即102倍时,pH=3,故答案为:3;
(2)pH=a的强酸加水稀释至原来体积的10b倍,则溶液的pH变为a+b(当a+b>7时,让pH=7),将pH=6的盐酸加水稀释至100倍即102倍时,由于6+2=8>7,故稀释后pH=7,故答案为:7;
(3)pH=a的弱酸加水稀释至原来体积的10b倍时,则溶液的pH<a+b,因为加水促进了弱电解质的电离,故溶液中的氢离子浓度下降的比较慢.故将pH=1的CH3COOH溶液稀释至100倍,pH<3,说明醋酸是弱酸,故答案为:小于3,弱.
点评 本题考查了溶液pH的计算,注意掌握酸的强弱对溶液pH的计算方法的影响,注意加水稀释促进弱电解质的电离,题目难度不大.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ②①②③ | B. | ①②②③ | C. | ②③②① | D. | ①①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.28g | B. | 1.4g | C. | 1.68g | D. | 2.1g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )| X | Y | Z | W | |
| A | C | CO | CO2 | Na2CO3 |
| B | Fe3O4 | Fe | FeCl2 | FeCl3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
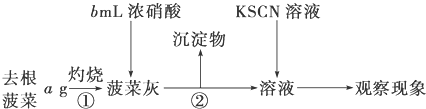
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
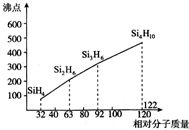 太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.
太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com