
| A、7.8 g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA |
| B、1 mol?L-1的碳酸钠溶液中含有CO32-的数目小于NA |
| C、标准状况下,2.24LCl2溶于水,转移的电子数目为0.1NA |
| D、1molNa被完全氧化生成Na2O2,失去个2 NA电子 |


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
A、C8H18(1)+
| ||||
B、C8H18(1)+
| ||||
| C、H+(aq)+OH-(aq)═H2O(aq);△H=一57.3 kJ?mol-1 | ||||
D、NaOH(aq)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业上用电解熔融氯化钠的方法制取钠 |
| B、钠加入氯化镁的饱和溶液中可以制取金属镁 |
| C、电解冶炼铝的原料是氯化铝 |
| D、碳在高温下能还原氧化镁中的镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O?Al(OH)3(胶体)+3H+ |
| B、“血液渗析”利用了胶体的性质 |
| C、沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
| D、工农业生产中的土壤保肥、冶金选矿、原油脱水、高压除尘等都与胶体的性质有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯的结构简式:C2H4 | ||
B、中子数为146、质子数为92的铀(U)原子
| ||
C、氯原子的结构示意图: | ||
D、氢氧根离子的电子式: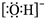 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2 L H2O屮所含的分子数为0.5 NA |
| B、常温下,32 g O3中所含的原子数为2 NA |
| C、1 mol?L-1 NaOH溶液中所含Na+离子数为NA |
| D、5.6 g Fe与2.24 L Cl2充分反应,转移的电子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com